Какова структура вируса? Как вирус проникает в клетку? Как происходит его размножение (репликация)?
Пользуясь порталом «ГОРОДСКОЙ РОДИЛЬНЫЙ ДОМ»,
Вы автоматически соглашаетесь с Правилами публикаций отзывов на сайте roddom-chita.ru
1.Общие положения:
1.1. Настоящие Правила регламентируют порядок размещения отзывов посетителей (пользователей) сайта roddom-chita.ru (далее – Сайт).
1.2. Посетители, приславшие отзывы для размещения на Сайте, (авторы отзывов), безвозмездно передают Администрации Сайта право свободного использования и предоставления широкого доступа к этим отзывам в пределах данного ресурса. Администрация Сайта оставляет за собой право использовать отзыв по собственному усмотрению и размещать его на других ресурсах (в печатных изданиях, на электронных носителях и т.д.).
2. Порядок публикации отзывов:
2.1. Администрация Сайта вправе самостоятельно и без уведомления пользователей отбирать отзывы для публикации, самостоятельно определять срок, в течение которого отзывы будут считаться актуальными.
2.2. До публикации отзыв проверяется Администрацией Сайта на соответствие настоящим Правилам, после чего Администрация Сайта принимает решение о его публикации.
2.3. Отзывы публикуются и используются без редактирования и поправок с сохранением авторской грамматики и пунктуации. Исключение составляет исправление явных опечаток.
2.4. В отзывах допускается только констатация и описание фактов, которые произошли с автором отзыва при обращении в ГУЗ «Городской родильный дом»
2.5. Отзывы без указания контактных данных (реальный e-mail пользователя, номер телефона и т.д.) считаются анонимными и на сайте не размещаются. В случае размещения такого отзыва, он наделяется пометкой: «Анонимный отзыв. Может содержать сведения, полностью не соответствующие действительности».
2.6. При размещении отзыва на Сайте администрация указывает исключительно имя автора отзыва. Контактные данные (реальный e-mail пользователя, номер телефона и т.д.) на страницах Сайта не указываются и не отображаются.
Контактными данными автора отзыва может воспользоваться исключительно Администрация сайта roddom-chita.ru для уточнения каких-либо данных, связанных с рассмотрением отзыва.
2.7. Администрация Сайта оставляет за собой право не публиковать отзыв пользователя, а также удалить с Сайта любой ранее опубликованный отзыв без объяснения причин и предупреждений в любое время.
2.8. В случае, если пользователь в будущем пожелает удалить свой отзыв с сайта roddom-chita.ru, он должен отправить запрос на удаление по адресу [email protected].
3. На сайте roddom-chita.ru не публикуются отзывы:
3.1. содержащие информацию, являющуюся клеветнической, дискредитирующей или угрожающей;
3.2. содержащие информацию, оскорбляющую честь и достоинство, а также национальные и религиозные чувства людей;
3.3. содержащие имена и другие персональные данные конкретных личностей, за исключением фамилии, имени, отчества медицинского работника ГУЗ «Городской родильный дом», в отношении которого написан отзыв;
3. 4. содержащие ненормативную лексику, высказывания оскорбительного характера и т.д.;
4. содержащие ненормативную лексику, высказывания оскорбительного характера и т.д.;
3.5. представляющие собой явную коммерческую рекламу, содержащие спам, контакты организаций и ссылки на сайты;
3.6. содержащие информацию, не относящуюся к деятельности ГУЗ «Городской родильный дом»;
3.7. содержащие призывы или агитацию не пользоваться услугами ГУЗ «Городской родильный дом»;
3.8. содержащие заведомо недостоверную информацию, призванную оттолкнуть клиентов от ГУЗ «Городской родильный дом»;
3.9. содержащие информацию о сравнении ГУЗ «Городской родильный дом» с другими юридическими лицами;
3.10. содержащие ссылки на отзывы, размещенные пользователями на других сайтах;
3.11. малоинформативные и необъективные.
4. Ответственность:
4.1. За содержание и достоверность информации в отзывах, размещаемых пользователями на сайте roddom-chita.ru, а также за нарушение прав третьих лиц, пользователь, разместивший данную информацию, несет ответственность самостоятельно.
4.2. Портал roddom-chita.ru, не является соавтором и распространителем данной информации, а лишь предоставляет площадку для ее размещения. Публикация отзыва на сайте не означает, что мнение Администрации сайта совпадает с мнением посетителя, оставившего отзыв. Администрация сайта не несет ответственности за достоверность сведений, содержащихся в отзывах.
4.3. В случае, возникновения претензий к пользователям, разместившим информацию, о достоверности размещенной информации, а также в случае, если размещенная информация, нарушает чьи либо права, портал обязуется, согласно действующему законодательству Российской Федерации, раскрыть всю имеющуюся информацию о данном пользователе (контактные данные (e-mail пользователя, номер телефона и т.д.)), в срок, предусмотренный законом.
5. Прочие условия:
5.1. Администрация сайта roddom-chita.ru оставляет за собой право на внесение изменений и дополнений в настоящие Правила в любой момент времени без уведомления посетителей (пользователей) Сайта. Изменения вступают в силу с момента их публикации.
Изменения вступают в силу с момента их публикации.
Генитальная ВПЧ-инфекция — информационный бюллетень центра по контролю и профилактике заболеваний
Вирус папилломы человека (ВПЧ) является наиболее распространенной инфекцией, передаваемой половым путем, в Соединенных Штатах. Вакцина может предотвратить некоторые последствия для здоровья, вызываемые ВПЧ.
Что такое ВПЧ?
ВПЧ является наиболее распространенной инфекцией, передаваемой половым путем (ИППП). ВПЧ — другой вирус, нежели ВИЧ(https://www.cdc.gov/hiv/basics) и ВПГ(https://www.cdc.gov/std/herpes/stdfact-herpes.htm) (герпес). 79 миллионов американцев, большинство в подростковом возрасте и ближе к 20 годам, заражены ВПЧ. Существует много различных видов ВПЧ. Некоторые виды могут вызывать проблемы со здоровьем, включая генитальные бородавки и рак. Для профилактики таких проблем со здоровьем существуют вакцины.
Как передается ВПЧ?
Вы можете заразиться ВПЧ посредством сексуального контакта (вагинального, анального или орального) с кем-либо, кто инфицирован этим вирусом. Как правило, им заражаются во время вагинального или анального секса. ВПЧ может передаваться и тогда, когда инфицированный человек не испытывает никаких признаков или симптомов.
Как правило, им заражаются во время вагинального или анального секса. ВПЧ может передаваться и тогда, когда инфицированный человек не испытывает никаких признаков или симптомов.
Любой сексуально активный человек может заразиться ВПЧ, даже если у вас был секс только с одним человеком. Симптомы могут развиться через много лет после того, как у вас был секс с инфицированным человеком, поэтому трудно понять, когда именно вы заразились.
Вызывает ли ВПЧ проблемы со здоровьем?
В большинстве случаев ВПЧ проходит сам по себе и не вызывает никаких проблем со здоровьем. Но когда ВПЧ не проходит, это может вызвать проблемы со здоровьем, такие как генитальные бородавки и рак.
Генитальные бородавки обычно появляются в виде маленького бугорка или группы бугорков в области половых органов. Они могут быть маленькими или большими, выступающими или плоскими или в форме, напоминающей цветную капусту. Лечащий врач может обычно диагностировать бородавки, осмотрев область гениталий.
Вызывает ли ВПЧ рак?
ВПЧ может вызвать рак шейки матки и других виды рака, включая рак наружных половых органов, влагалища, пениса или заднего прохода. Он также может вызывать рак задней стенки горла, в том числе рак основания языка и миндалин (так называемый рак ротоглотки).(https://www.cdc.gov/cancer/hpv/statistics/headneck.htm)
Зачастую проходят годы, даже десятилетия, прежде чем после инфицирования ВПЧ у человека развивается рак. Виды ВПЧ, которые могут вызывать генитальные бородавки, не являются теми видами ВПЧ, которые могут вызывать раковые заболевания.Невозможно узнать, у каких людей, заразившихся ВПЧ, будет рак или другие проблемы со здоровьем. Люди со слабой иммунной системой (в том числе с ВИЧ/СПИДом) менее способны бороться с ВПЧ. У них также могут с большей вероятностью развиться проблемы со здоровьем от ВПЧ.
Как я могу избежать ВПЧ и проблем со здоровьем, которые он может вызвать?
Чтобы снизить вероятность заражения ВПЧ, вы можете предпринять несколько мер:
Пройти вакцинацию. Вакцины против ВПЧ являются безопасными и эффективными. При использовании в рекомендуемых возрастных группах они могут защитить от болезней (включая рак), вызываемых ВПЧ. (См. раздел «Кто должен получать прививки?» ниже.) Центр по контролю и профилактике заболеваний рекомендует детям от 11 до 12 лет принять две дозы вакцины против ВПЧ для защиты от рака, вызванного ВПЧ. Дополнительную информацию о рекомендациях см. на странице https://www.cdc.gov/vaccines/vpd/hpv/public/index.html
Вакцины против ВПЧ являются безопасными и эффективными. При использовании в рекомендуемых возрастных группах они могут защитить от болезней (включая рак), вызываемых ВПЧ. (См. раздел «Кто должен получать прививки?» ниже.) Центр по контролю и профилактике заболеваний рекомендует детям от 11 до 12 лет принять две дозы вакцины против ВПЧ для защиты от рака, вызванного ВПЧ. Дополнительную информацию о рекомендациях см. на странице https://www.cdc.gov/vaccines/vpd/hpv/public/index.html
Пройти скрининг на рак шейки матки. Рутинный скрининг для женщин в возрасте от 21 до 65 лет может предотвратить рак шейки матки.
Если вы сексуально активны:
- правильно(https://www.cdc.gov/condomeffectiveness/male-condom-use.html) используйте латексные презервативы каждый раз, когда вы занимаетесь сексом. Это может снизить вероятность заражения ВПЧ. Но ВПЧ может инфицировать участки, не защищенные презервативом — таким образом, презервативы не могут в полной мере защитить от заражения ВПЧ;
- поддерживайте взаимно моногамные отношения — или занимайтесь сексом только с тем, кто занимается сексом только с вами.

Кто должен получать прививки?
Все мальчики и девочки в возрасте 11–12 лет должны получить прививку.
Если прививки не были сделаны в более молодом возрасте, можно сделать их позже. Подросткам и мужчинам рекомендуются делать прививки до 21 года, а девушками и женщинам — до 26 лет.
Вакцинация также рекомендуется для геев и бисексуалов (или любого человека, который занимается сексом с мужчиной) до 26 лет. Кроме того, вакцинация рекомендуется для мужчин и женщин с ослабленной иммунной системой (в том числе и людей с ВИЧ/СПИДом) до 26 лет, если они не были полностью привиты ранее.
Как я узнаю, что у меня ВПЧ?
Не существует такого анализа, с помощью которого можно было бы выяснить «статус ВПЧ» у человека. Кроме того, не существует утвержденного анализа на обнаружение ВПЧ во рту или горле.
Имеются тесты на ВПЧ, которые могут использоваться для скрининга рака шейки матки. Такие тесты рекомендуются для проведения скрининга только у женщин в возрасте 30 лет и старше.
Большинство людей с ВПЧ не знают, что они инфицированы, и у них никогда не проявляются какие-либо симптомы, и нет никаких проблем со здоровьем в результате инфицирования. Некоторые люди обнаруживают, что у них есть ВПЧ, когда у них появляются генитальные бородавки. Женщины могут узнать, что они заражены ВПЧ, когда получают аномальный результат ПАП-теста (во время скрининга на рак шейки матки). Другие же люди могут обнаружить только тогда, когда у них появляются более серьезные проблемы в результате заражения ВПЧ, например, рак.
Как часто встречается ВПЧ и проблемы со здоровьем, вызванные ВПЧ?
ВПЧ (вирус). Около 79 миллионов американцев в настоящее время инфицированы ВПЧ. Около 14 миллионов человек заражаются каждый год. ВПЧ настолько распространен, что почти каждый сексуально активный человек заражается ВПЧ в какой-то момент своей жизни, если не получает соответствующую вакцину.
Проблемы со здоровьем, связанные с ВПЧ, включают генитальные бородавки и рак шейки матки.
Генитальные бородавки. До появления вакцины против ВПЧ приблизительно от 340 000 до 360 000 женщин и мужчин страдали от генитальных бородавок, вызванных ВПЧ, ежегодно.* Кроме того, примерно у одного из 100 сексуально активных взрослых в США были/есть генитальные бородавки в какой-то момент времени.
Рак шейки матки. Ежегодно почти у 12 000 женщин, проживающих в США, диагностируется рак шейки матки, и более 4000 женщин умирают от рака шейки матки — даже при скрининге и лечении.
Есть и другие заболевания и виды рака(https://www.cdc.gov/std/hpv/stdfact-hpv.htm), вызванные ВПЧ, которыми страдают люди, живущие в Соединенных Штатах. Каждый год приблизительно 19 400 женщин и 12 100 мужчин страдают от рака, вызванного ВПЧ.
* Эти цифры включают только тех людей, которые обращались к врачу за лечением генитальных бородавок. Реальное количество людей, страдающих генитальными бородавками, может быть значительно больше.
Я беременна. Повлияет ли ВПЧ на мою беременность?
Если вы беременны и у вас ВПЧ, у вас могут образоваться генитальные бородавки или произойти аномальные изменения клеток шейки матки. Аномальные изменения в клетках можно обнаружить при проведении рутинного скрининга на рак шейки матки. Вы должны пройти рутинный скрининг на рак шейки матки, даже если вы беременны.
Могу ли я вылечиться от ВПЧ и избавиться от проблем со здоровьем, вызванных ВПЧ?
Не существует лекарства от самого вируса. Тем не менее, существует лечение проблем со здоровьем, которые могут быть вызваны ВПЧ:
- Генитальные бородавки можно вылечить, обратившись к вашему поставщику медицинских услуг, или с помощью отпускаемых по рецепту лекарств. Если их не лечить, генитальные бородавки могут исчезнуть, остаться такими же или увеличиваться в размерах или количестве.
- Предраковое состояние шейки матки можно вылечить. Женщины, которые регулярно сдают мазок на ПАП-тест, и проходят необходимое последующее наблюдение, могут выявить проблемы до того, как появится рак.
 Профилактика всегда лучше, чем лечение. Для получения дополнительных сведений посетите сайт www.cancer.orgExternal.
Профилактика всегда лучше, чем лечение. Для получения дополнительных сведений посетите сайт www.cancer.orgExternal. - Другие виды рака, связанные с ВПЧ, также лучше поддается лечению, когда они диагностируются и их лечение начинается на ранних стадиях. Для получения дополнительных сведений посетите сайт www.cancer.orgExternal.
Вирус Коксаки: эпидемиология, клиника, профилактика
Энтеровирусные инфекции – большая группа острых вирусных заболеваний, вызываемых энтеровирусами группы Коксаки и ECHO, характеризующихся многообразием клинических проявлений от легких лихорадочных состояний до тяжелых менингитов.
Энтеровирусы распространены повсеместно, устойчивы во внешней среде и длительное время могут сохраняться в сточных водах, плавательных бассейнах, открытых водоемах, предметах обихода, продуктах питания (молоко, фрукты, овощи). Вирус быстро погибает при прогревании, кипячении.
Возможные пути передачи инфекции: фекально-оральный (пищевой и водный), воздушно-капельный, контактно-бытовой (грязные руки, игрушки).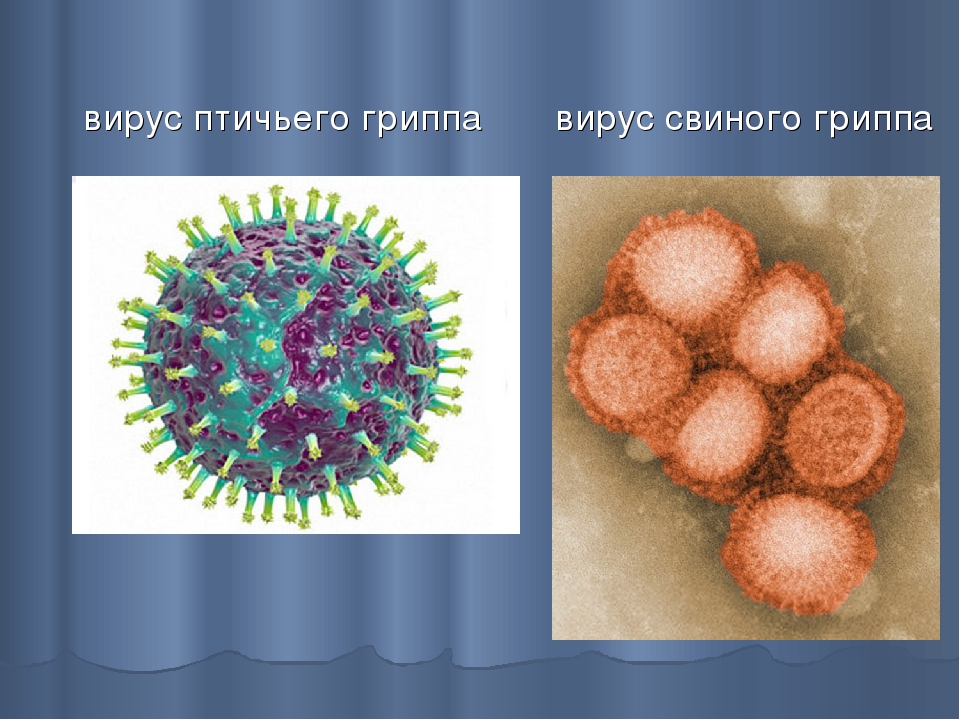 Энтеровирусные инфекции характеризуются быстрым распространением заболевания среди людей.
Энтеровирусные инфекции характеризуются быстрым распространением заболевания среди людей.
Источником инфекции являются больные люди, в том числе бессимптомной формой, и вирусоносители. Наиболее интенсивно вирусы выделяются от человека в первые дни болезни, однако возможно их выделение до нескольких месяцев.
Восприимчивость людей к вирусу высокая. Часто наблюдаются групповые заболевания, возможны семейные вспышки
Заболевание начинается остро, с подъема температуры тела до 39-40 градусов. Появляется сильная головная боль, головокружение, рвота, иногда боли в животе, спине, у детей возможен судорожный синдром, нередко выраженные катаральные проявления со стороны ротоглотки, верхних дыхательных путей, болезненные высыпания на коже. Серозный вирусный менингит является наиболее типичной и тяжелой формой энтеровирусной инфекции. При появлении перечисленных жалоб необходимо срочно изолировать больного, так как он является источником заражения для окружающих, и обратиться к врачу.
Несмотря на яркую клинику и выраженность проявлений течение энтеровирусной инфекции благоприятное, осложнения встречаются редко.
Меры личной профилактики должны заключаться в соблюдении правил личной гигиены, соблюдении питьевого режима (кипяченая вода, бутилированная вода), тщательной обработки употребляемых фруктов, овощей и последующим ополаскиванием кипятком. Рекомендуется влажная уборка жилых помещений не реже 2 раз в день, проветривание помещений.
Ни в коем случае не допускать посещения ребенком организованного детского коллектива с любыми проявлениями заболевания.
При первых признаках заболевания необходимо немедленно обращаться за медицинской помощью, не заниматься самолечением!
Как удалить вирус восстановления компьютера
Симптомы
При просмотре Интернета или работы на компьютере после в Интернете, вы можете заметить может открыться новое окно с названием Восстановление компьютера , задаваемые для дефрагментации вашего компьютера и затем запрашивает личную информацию как ваш адрес электронной почты.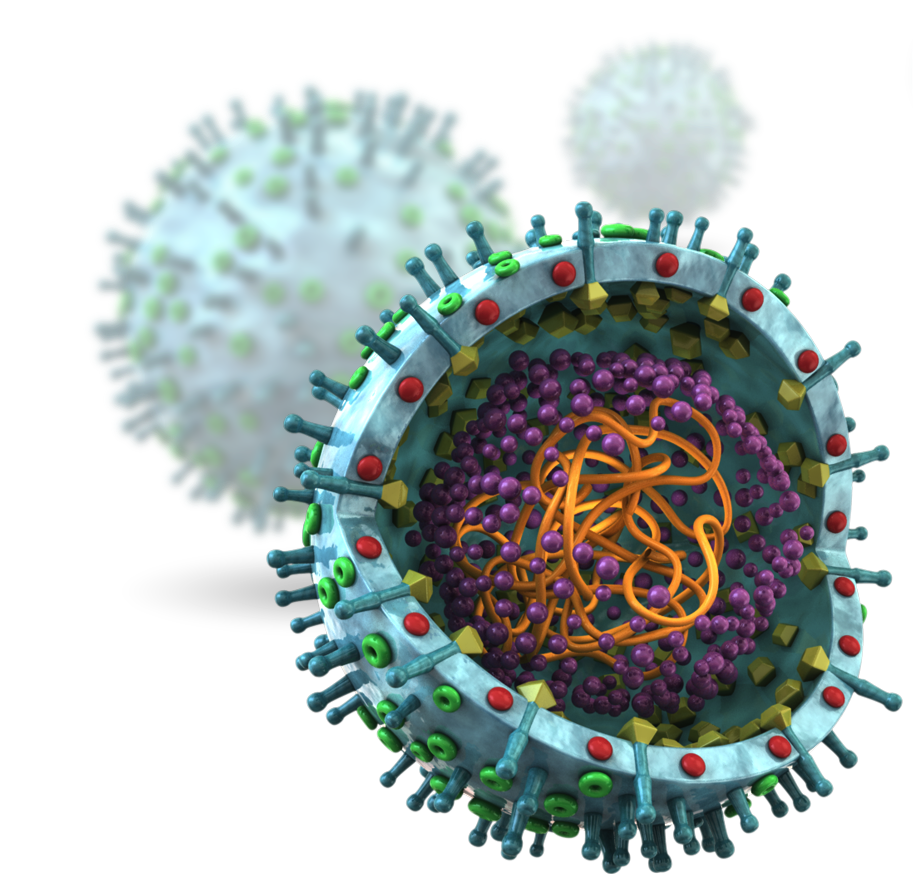 Этот вариант вредоносная программа Win32/FakeSysdef и может удалить или скрыть файлы, а также принять участие в других вредоносных действий на компьютере.
Этот вариант вредоносная программа Win32/FakeSysdef и может удалить или скрыть файлы, а также принять участие в других вредоносных действий на компьютере.
Решение
Эту проблему можно разрешить и восстановление компьютера вирус удален, запустив средство проверки безопасности Microsoft. Чтобы сделать это, выполните следующие действия:
-
Перейти к http://www.microsoft.com/security/scanner/en-us/default.aspxи нажмите кнопку « Загрузить ».
-
Следуйте инструкциям на экране для загрузки и установки Средство проверки безопасности Microsoft. В ответ на приглашение сохраните файл на рабочем столе.
-
Перезагрузите компьютер и загрузки в Безопасном режиме:
Для Windows 7, Windows Vista и Windows XP:
-
При запуске компьютера, несколько раз нажмите клавишу F8 .

-
Появится Меню дополнительных вариантов загрузки Windows (Windows XP) или в меню Дополнительные варианты загрузки (Windows Vista или Windows 7) . Выберите Безопасный режим и нажмите клавишу Ввод .
-
Если предлагается ввести учетные данные администратора , введите Имя пользователя и пароль и нажмите кнопку ОК.
-
-
Дважды щелкните значоксканера Безопасности Microsoftна рабочем столе. Может быть указан как msert.
-
Щелкните поле рядом с кнопкой принять все условия лицензионного соглашения, а затем нажмите кнопку Далее.
-
Нажмите кнопку Быстрого сканирования, а затем нажмите кнопку Далее.
-
Средство проверки безопасности Microsoft будет проверять компьютер.
 Это может занять несколько минут. После завершения нажмите кнопку просмотреть подробные результаты сканирования. Вы должны увидеть троянских: Win32/FakeSysdef перечисленные в области результатов.
Это может занять несколько минут. После завершения нажмите кнопку просмотреть подробные результаты сканирования. Вы должны увидеть троянских: Win32/FakeSysdef перечисленные в области результатов.
Дополнительные сведения
Дополнительные сведения о средство проверки безопасности Microsoft: http://www.microsoft.com/security/scanner/en-us/default.aspx
Дополнительные сведения о вредоносная программа Win32/FakeSysdef и его разновидностях: http://www.microsoft.com/security/portal/Threat/Encyclopedia/Entry.aspx?name=Trojan%3aWin32%2fFakeSysdef&threatid=4295122934
Корпорация Майкрософт предлагает программу бесплатно безопасности Microsoft Security Essentials, которые помогут защитить компьютер от заражения вирусом вредоносных программ. Для получения дополнительной информации о Microsoft Security Essentials, посетите: http://www.microsoft.com/en-us/security_essentials/default. aspx
aspx
Для получения сведений о том, как защитить компьютер от хакеров, вредоносных программ и других вредоносных действий посетите безопасности и центр обеспечения безопасности в корпорации Майкрософт: http://www.microsoft.com/security/default.aspx
Что такое вирус, где он живет и чего хочет — объясняем сложные вещи простыми словами | Громадское телевидение
1
Что такое вирусы?
Это первые живые организмы на планете и одновременно — провокаторы болезней.
Возбудители заболеваний бывают разные: в виде клетки (это бактерии), в более мелкой форме — это вирусы.
Но не думайте, что вирусы — какие-то простаки по сравнению с бактериями. Это не так, ведь они живые, у них есть ДНК или РНК, они способны к мутациям, размножению и выживанию в сложных условиях.
2
Когда возникли вирусы и в чем их польза?
Считается, что вирусы являются аборигенами нашей планеты.
Есть версия, что они попали на Землю в момент ее создания, потому что они живут и в космосе.
Если принимать во внимание, что с вирусов началась жизнь на нашей планете, то вирусы — это хорошо.
Когда-то эксперимент доказал, что в условиях полной стерильности организм является нежизнеспособным. Это доказывает необходимость для нас контактировать с вирусами. Они суперважны для иммунной системы.
Вы знаете, что у медиков существует понятие «сопливый возраст»?
Он длится от 2 до 9 лет, когда дети часто болеют. Это абсолютно нормальный процесс для нашей жизни. Так дети знакомятся с вирусами, производят против них естественное оружие (иммунитет) и адаптируются к жизни на планете.
Чтобы мы создавали больше важных материалов для вас, поддержите hromadske на платформе Спільнокошт. Любая помощь имеет большое значение.
3
С чем их не стоит путать и почему?
Вирусы нельзя путать с бактериями, особенно во время лечения.
Например, антибиотики не лечат от вирусов. Антибиотики существуют для лечения от бактерий.
Вирусы — это, например, грипп, простуда, корь, свинка, краснуха, полиомиелит.
А бактериальные болезни — это, например, туберкулез, тиф, холера или ангина.
Бактерии вызывают другие симптомы и характер развития болезни, чем вирусы. Потому что это сложная форма жизни.
4
А где живут вирусы и что они любят?
Вирусы больше всего любят жить в живом организме — человека, животного или растения. Именно в организме вирусы занимаются любимым делом — размножением.
Но они умеют выживать и вне организма. В основном где-то на дверных ручках, столах, перилах маршруток и других поверхностях.
Продолжительность их жизни вне организма зависит от благоприятности условий. Вирусы любят низкую температуру, влажность, туман. При таких условиях им легко мигрировать от человека к человеку.
5
Как и для чего вирусы попадают в организм?
Для размножения. Потому что самовоспроизводство — это смысл их жизни. Лишь в организме вирусы могут продолжать свой род, ведь для этого им нужна клетка.
Стоит понимать, что вирусы не появляются у людей из-за забытой дома шапки, холодного лимонада или расстегнутой куртки.
В природе вирусы живут всегда, но погода влияет на их способность выживать вне организма и быстро мигрировать от человека к человеку.
Словом, нынешняя зима — идеальное время для вирусных заболеваний.
6
Как спастись от вирусов?
Обязательный шаг номер один — вакцинация.
Универсальной вакцины не существует. Отдельные вакцины спасают, например, от вирусных болезней, которые называют «обязательными» в жизни человека: краснухи, ветрянки, кори и тому подобных. Избежать этих вирусов — уже большая победа. К сожалению, до сих пор люди иногда умирают от кори или полиомиелита.
Шаг номер два — гигиена.
Как вы уже знаете, вирусы могут жить на разных поверхностях. Коснуться дверной ручки, на которой находится вирус, а затем облизать палец или почесать глаза — значит заболеть.
Защититься от вирусов помогает комплексный подход, говорит иммунолог Федор Лапий. «Сопливый возраст» тренирует иммунную систему, вакцинация уберегает от «обязательных» болезней, а гигиена и осторожность — наши элементарные меры безопасности:
«Сопливый возраст» тренирует иммунную систему, вакцинация уберегает от «обязательных» болезней, а гигиена и осторожность — наши элементарные меры безопасности:
«Маска нужна больному, чтобы не инфицировать других. Ваши чистые руки имеют значение и для других людей. Поэтому здесь вопрос социального договора, иными словами — ответственности».
Новый штамм коронавируса: что мы о нем знаем?
- Джеймс Галлахер
- Корреспондент Би-би-си по вопросам науки и медицины
Автор фото, PA Media
Быстрое распространение нового штамма коронавируса вызвало введение жесткого локдауна в Лондоне и на юго-востоке Англии, отменило рождественские послабления для жителей Англии, Шотландии и Уэльса и заставило ряд стран, включая и Россию, ввести запрет на авиасообщение с Великобританией.
Как же так произошло, что за считанные месяцы вирус так мутировал, что заставил власти принять экстренные меры?
Научный совет, консультирующий британские власти, «с определенной долей уверенности» заявляет, что новый штамм легче передается от человека к человеку, чем прежние.
Пока многое еще непонятно, поскольку новый штамм изучен мало.
Я писал раньше, что вирусы постоянно мутируют, и потому чрезвычайно важно постоянно следить за тем, как они себя ведут.
Почему этот новый штамм вызывает опасения?
Совокупность трех факторов привлекает особое внимание ученых:
- Он быстро вытесняет другие штаммы этого же вируса;
- Мутация происходит в таких частях вируса, которые представляют особую важность;
- Некоторые из этих мутаций уже продемонстрировали в лабораторных условиях повышенную способность вируса проникать в клетки.
Все это вместе предполагает, что вирус может быстрее распространяться.
Тем не менее абсолютной уверенности в этом у нас пока нет.
Новые штаммы могут становиться более распространенными только по той причине, что оказываются в нужном месте в нужное время. Например, в Лондоне, где до недавнего времени действовал второй уровень ограничений.
Например, в Лондоне, где до недавнего времени действовал второй уровень ограничений.
Введение четвертого, наивысшего уровня ограничений объясняется стремлением сократить распространение этого нового варианта.
«Нужно проводить лабораторные исследования. Но будем ли мы ждать недели, а то и месяцы? Вероятно, нет, учитывая нынешние обстоятельства», — пояснил Би-би-си логику событий профессор Ник Ломан из британской медицинской Ассоциации по расшифровке генома нового коронавируса (Covid-19 Genomics UK Consortium).
Насколько быстро он распространяется?
Впервые этот новый штамм был выявлен в сентябре.
Уже в ноябре примерно 25% всех заражений в Лондоне были как раз этим вариантом коронавируса. А к середине декабря их стало более 65%.
На примере результатов тестов, сделанных в британской лаборатории Milton Keynes Lighthouse Laboratory, мы видим, как этот штамм стал доминировать в лабораторных анализах.
Математики пытаются рассчитать поведение других штаммов коронавируса, чтобы понять, насколько более агрессивен может быть новый.
Однако тут надо учитывать не только поведение самого вируса, но и то, как будут вести себя люди.
Премьер-министр Борис Джонсон сказал, что новый штамм может быть на 70% заразнее, и именно по этой причине на 0,4 может вырасти индекс репродукции (который показывает, растет ли число заражений или убывает) .
Об этих 70% рассказал в минувшую пятницу доктор Эрик Фольц из Имперского колледжа Лондона. Во время выступления он сказал: «Пока еще слишком рано делать выводы… но из того, что мы уже видим, он распространяется очень быстро, гораздо быстрее, так что важно продолжать наблюдать за ним.»
Нет никакой определенной цифры, которая бы с точностью указывала на то, насколько более заразен этот новый штамм.
Ученые, которые еще не обнародовали данные своих исследований, называли мне как гораздо более высокий процент, так и значительно более низкий, чем 70%.
И остается еще вопрос по поводу того, действительно ли он более заразный, чем прежние варианты?
«Тех данных, которые имеются в открытом доступе, совершенно недостаточно для того, чтобы сделать четкий и безусловный вывод о том, что заразность у вируса стала выше», — говорит профессор Джонатан Болл, вирусолог из Ноттингемского университета.
Насколько широко он распространился?
На сегодняшний день полагают, что этот штамм либо возник у пациента в Великобритании, либо был завезен из другой страны, где за мутациями коронавируса особенно не следят.
Этот штамм сейчас обнаруживается по всему Соединенному Королевству за исключением Северной Ирландии, с концентрацией в Лондоне, а также в графствах на юге и востоке Англии. В других районах, кажется, он не очень прижился.
Данные международного проекта Nextstrain, следящего за генетическим кодом всех вирусных образцов со всего мира, позволяют предположить, что новый штамм коронавируса, появившийся в Дании и Австралии, пришел из Британии.
Нидерланды тоже зафиксировали несколько случаев этого штамма.
Схожий вариант, возникший в Южной Африке, имеет некоторые характеристики, присущие новому штамму, но, по всей видимости, не связан с британским.
Случались ли подобные мутации ранее?
Да. Коронавирус, впервые выявленный в китайском городе Ухань, — не тот, который обнаруживается сейчас по всему миру.
Другой, A222V, распространился по всей Европе с отдыхавшими этим летом в Испании.
Что мы знаем о мутациях британского штамма?
Изменения касаются шиповидного белка — своего рода ключа, которым вирус отмыкает дверцу в клетки.
Одна из мутаций, N501Y, ответственна за самую важную часть этого шипа, известную как рецептор-связывающий домен (RBD).
Именно здесь шип впервые входит в контакт с поверхностью клетки. Любые изменения, которые помогут вирусу проникать внутрь, вероятнее всего, дадут этому штамму преимущество.
«По всем параметрам похоже, что это важная адаптация,» — отмечает профессор Ломан.
Неоднократно фиксировалась и еще одна мутация (делеция H69/V70), — в частности, у зараженных норок на фермах в Дании, — в ходе которой происходит уничтожение крошечной части шипа.
Исследования, проводимые профессором Рави Гуптой из Кембриджского университета, показывают, что в лабораторных условиях эта мутация увеличивает в два раза инфекционность коронавируса.
Автор фото, Getty Images
Подпись к фото,Изменения касаются шиповидного белка — своего рода ключа, которым вирус отмыкает дверцу в клетки
В ходе этих же экспериментов ученые предположили, что эти мутации делают менее эффективными лечение больных с помощью переливания крови пациентов, переболевших ковидом.
«Случаи все растут и растут, и это беспокоит правительство, беспокоит нас, беспокоит всех ученых», — сказал профессор Гупта в интервью Би-би-си.
Откуда пришел новый штамм?
Этот штамм претерпел неожиданно много мутаций.
Наиболее вероятное тому объяснение таково, что он возник у пациента с ослабленной иммунной системой, который не смог побороть этот вирус.
Вместо этого организм этого человека стал своего рода благоприятной средой для мутации коронавируса.
Стал ли ковид более смертельным?
Пока нет никаких свидетельств тому, что это может быть так. Но ситуацию надо держать под контролем.
Однако даже сам факт того, что зараженных становится больше, может создать проблемы в больницах.
Если новый вариант будет легче передаваться, большему числу пациентов понадобится лечение в стационаре.
Будут ли эффективны вакцины против нового штамма?
Практически точно можно сказать — да. Во всяком случае на ближайшее будущее.
Все три ведущие мировые вакцины вызывают иммунный ответ организма на существующий спайк-белок коронавируса.
Они настраивают иммунную систему на то, чтобы она атаковала различные составляющие вируса, а это значит, что даже несмотря на то, что часть шипа мутировала, вакцины по-прежнему будут эффективны.
«Однако если мы прозеваем еще ряд мутаций, тогда надо будет волноваться», — говорит профессор Гупта.
«Этот вирус потенциально настроен на то, чтобы обойти защиту, даваемую вакциной. Он уже сделал к этому ряд шагов,» — говорит ученый.
Подобное может произойти, если вирус мутирует настолько, что вакцина оказывается бездейственна, а вирус продолжает заражать людей.
И это, вероятно, вызывает больше всего опасений в связи с новым коронавирусом и, в частности, с новым штаммом, показывающим, что он способен адаптироваться так, чтобы заражать все большее число людей.
И тогда мы окажемся в такой же ситуации, что и при гриппе, когда вакцину необходимо регулярно видоизменять.
К счастью, те вакцины против коронавируса, которые мы уже получили, легко поддаются этому.
как создают биологическое оружие массового поражения и где используют
Вирусы уже очень давно изучают в лабораториях, а также выводят полученные с нуля виды или иначе говоря de novo. Однако работа вирусологов массово заинтересовала широкую общественность только после начала пандемии коронавируса. Рассказываем, с какой целью выводят биологическое оружие, есть ли у модифицированных вирусов положительные задачи и что известно о происхождении коронавируса.
Искусственные вирусы
Многие вирусы могут быть получены de novo, то есть с нуля, а первый искусственный вирус был создан в 2002 году. Несмотря на некоторые неправильные трактовки, при этом процессе синтезируется не сам вирус как таковой, а его геномная ДНК (в случае ДНК-вирусов) или комплементарная копия ДНК его генома (в случае РНК-вирусов).
У вирусов многих семейств искусственная ДНК или РНК, если она введена в клетку, проявляет инфекционные свойства. Иными словами, такие вирусы содержат всю необходимую информацию для образования новых вирусов.
Иными словами, такие вирусы содержат всю необходимую информацию для образования новых вирусов.
Эту технологию в настоящее время используют для разработки вакцин нового типа. Возможность создавать искусственные вирусы имеет далеко идущие последствия, поскольку вирус не может вымереть, пока известна его геномная последовательность и имеются чувствительные к нему клетки.
В наши дни полные геномные последовательности 2408 различных вирусов (в том числе оспы) находятся в публичном доступе в онлайн-базе данных, поддерживаемой Национальными институтами здравоохранения США.
Микрофотография, показывающая цитопатические эффекты, вызванные вирусом простого герпеса первого типа. Тест ПапаниколауКак из вирусов делают биологическое оружие
Способность вирусов вызывать опустошительные эпидемии среди людей порождает беспокойство, что вирусы могут использоваться как биологическое оружие.
Биологическое оружие — это патогенные микроорганизмы или их споры, вирусы, бактериальные токсины, заражающие людей и животных, предназначенные для массового поражения живой силы и населения противника, сельскохозяйственных животных, посевов сельскохозяйственных культур, заражения продовольствия и источников воды, а также порчи некоторых видов военного снаряжения и военных материалов.
Биологическое оружие включает также средства доставки патогенных микроорганизмов и животных-переносчиков. Является оружием массового поражения и запрещено согласно Женевскому протоколу 1925 года.
Дополнительные опасения вызвало успешное воссоздание вредоносного вируса испанского гриппа в лаборатории. Другим примером может служить вирус оспы. Он на всем протяжении истории опустошал множество стран вплоть до его окончательного искоренения. Официально образцы вируса оспы хранятся лишь в двух местах в мире — в двух лабораториях в России и США.
Опасения, что он может быть использован как оружие, не совсем беспочвенны; вакцина против оспы иногда имеет тяжелые побочные эффекты — в последние годы до официально объявленного искоренения вируса больше людей серьёзно заболели из-за вакцины, чем от вируса, поэтому вакцинация против оспы больше не практикуется повсеместно. По этой причине большая часть современного населения Земли практически не имеет устойчивости к оспе.
Способы применения бактериальных и вирусных средств
Средствами доставки и способами применения биологического оружия, как правило, являются:
- боевые части ракет;
- авиационные бомбы;
- артиллерийские мины и снаряды;
- пакеты (мешки, коробки, контейнеры), сбрасываемые с самолетов;
- специальные аппараты, рассеивающие насекомых с самолетов;
- диверсионные методы.

Заболевание в этом случае может произойти в результате прямого контакта с заражёнными предметами. Возможно также преднамеренное оставление при отходе инфекционных больных с тем, чтобы они явились источником заражения.
При разрыве боеприпасов, снаряженных бактериальной рецептурой, образуется бактериальное облако, состоящее из взвешенных в воздухе мельчайших капелек жидкости или твёрдых частиц. Облако, распространяясь по ветру, рассеивается и оседает на землю, образуя заражённый участок, площадь которого зависит от количества рецептуры, её свойств и скорости ветра.
Проблемой является то, что вне природного очага обитания и без соответствующих его экологической обстановке механизмов передачи, возбудитель заболевания передаваться людям не будет.
Отпочковывание вируса от клетки-хозяинаОсобенности поражения биологическим оружием
При поражении бактериальными или вирусными средствами заболевание наступает не сразу, почти всегда имеется скрытый (инкубационный) период, в течение которого заболевание не проявляет себя внешними признаками, а пораженный не теряет боеспособности.
Некоторые заболевания (чума, холера, сибирская язва) способны передаваться от больного человека здоровому и, быстро распространяясь, вызывать эпидемии. Установить факт применения бактериальных средств и определить вид возбудителя достаточно трудно, поскольку ни микробы, ни токсины не имеют ни цвета, ни запаха, ни вкуса, а эффект их действия может проявиться через большой промежуток времени.
Обнаружение бактерий и вирусов возможно только путём проведения специальных лабораторных исследований, на что требуется значительное время, что затрудняет своевременное проведение мероприятий по предупреждению эпидемических заболеваний.
Признаком применения бактериологического оружия являются также валяющиеся на местности использованные боеприпасы (предназначенные для него) и другие средства его доставки. В некоторых случаях также — внезапное появление или резкое увеличение количества определенных насекомых или грызунов (например — блохи на снегу).
Современные стратегические средства биологического оружия используют смеси вирусов и спор бактерий для увеличения вероятности летальных исходов при применении, однако используются, как правило, штаммы, не передающиеся от человека к человеку, чтобы территориально локализовать их воздействие и избежать вследствие этого собственных потерь.
Искусственные вирусы можно использовать во благо
Ученые из NPL (Национальной физической лабораторией), работая с партнерами из Кембриджского и Эксетерского университетов, а также из Королевского колледжа Лондона, разработали создают искусственный вирус для борьбы с супербактериями
Рост числа супербактерий вызывает серьезную озабоченность в медицинском сообществе, поскольку бактерии эволюционируют, чтобы избежать существующих методов лечения быстрее, чем разрабатывают новые антибиотики. Вместо того чтобы создавать новые лекарства, группа экспертов пошла другим путем.
Авторы работы, опираясь на принципы архитектуры вируса, создали синтетический белок Ψ—капсид, который собирается из небольшого молекулярного мотива или характерной последовательности нуклеотидов (в ДНК, РНК) или аминокислот (в белках). Мотив нашли в клетках человека. Он может распознавать молекулярные паттерны, связанные с патогенами, на бактериальных поверхностях.
Отмечается, что благодаря комбинации наноразмерных и одноклеточных изображений, команда подтвердила, что капсиды наносят непоправимый ущерб бактериям. Капсиды были одинаково эффективны в любой из своих хиральных форм, что может сделать их невидимыми для иммунной системы хозяина, а также позволит убивать различные фенотипы бактерий и супербактерий без цитотоксичности in vitro и in vivo.
Капсиды были одинаково эффективны в любой из своих хиральных форм, что может сделать их невидимыми для иммунной системы хозяина, а также позволит убивать различные фенотипы бактерий и супербактерий без цитотоксичности in vitro и in vivo.
Коронавирус создан искусственно?
Пока нельзя сказать однозначно. Предлагаем ознакомиться с недавним необычном исследованием, в котором британский и норвежский ученые Ангус Далглиш и Биргер Сёренсен утверждают, что COVID-19 был создан в лаборатории.
Далглиш и Сёренсен обнаружили в вирусе «уникальные отпечатки пальцев» и свидетельство того, что он не имеет достоверного источника. Следовательно, как утверждают ученые, вирус мог появиться только в результате лабораторных манипуляций.
По их словам, ранее они уже пытались опубликовать результаты своего исследования, но были отвергнуты научными журналами, которые были уверены в естественном происхождении вируса. Сейчас в ряде стран снова заговорили о необходимости пересмотреть версии возникновения COVID-19, указывает издание.
Исследователи обратили внимание на эксперименты, проведенные в лаборатории в Ухане в период с 2002 по 2019 год, и выяснили, что
их китайские коллеги, некоторые из которых работают совместно с американскими университетами, занимались исследованиями по изменению вируса таким образом, чтобы повысить его заразность.
Авторы исследования считают, что за «основу» был взят коронавирус, обнаруженный у китайских пещерных летучих мышей и к нему добавлен новый «шип», в конечном итоге был получен более заразный и смертельный SARS-CoV-2.
О том, что с вирусом могли проводиться манипуляции, говорит обнаруженная Далглишем и Сёренсеном цепочка из четырех аминокислот, которые имеют положительный заряд. Это позволяет вирусу «плотно цепляться за отрицательно заряженные части человеческих клеток, как магнит, и за счет этого становиться более заразным», объяснил норвежский ученый.
Читать далее:
Поражение кожи, мозга и глаз: как COVID-19 проникает в человеческие органы
Самое таинственное природное явление. Откуда берется шаровая молния и чем она опасна?
Откуда берется шаровая молния и чем она опасна?
НАСА впервые показало ракету, которая отправит астронавтов на Луну
Вирусоподобные частицы: препараты, иммуногенность и их роль в качестве нановакцинов и наноносителей лекарств | Журнал нанобиотехнологий
Бай Б., Ху Кью, Ху Х, Чжоу П, Ши З, Мэн Дж и др. Вирусоподобные частицы SARS-подобного коронавируса, образованные мембранными белками различного происхождения, демонстрируют стимулирующую активность в дендритных клетках человека. PLoS ONE. 2008; 3 (7): e2685.
PubMed PubMed Central Статья CAS Google ученый
Chung YH, Cai H, Steinmetz NF. Вирусные наночастицы для доставки лекарств, визуализации, иммунотерапии и тераностики. Adv Drug Deliv Rev. 2020; 156: 214–35.
CAS PubMed PubMed Central Статья Google ученый
Steinmetz NF. Вирусные наночастицы как платформы для терапевтических средств и устройств визуализации нового поколения. Наномедицина. 2010. 6 (5): 634–41.
Наномедицина. 2010. 6 (5): 634–41.
CAS PubMed PubMed Central Статья Google ученый
Пушко П., Пампенс П., Гренс Э. Развитие технологии вирусоподобных частиц от небольших высокосимметричных до больших сложных структур вирусоподобных частиц. Интервирология. 2013. 56 (3): 141–65.
CAS PubMed Статья PubMed Central Google ученый
Байер М.Э., Блумберг Б.С., Вернер Б. Частицы, ассоциированные с австралийским антигеном, в сыворотке крови пациентов с лейкемией. Синдр Дауна Hepat Nat. 1968. 218 (5146): 1057–9.
CAS Google ученый
Latham T, Galarza JM. Образование частиц дикого типа и химерных вирусоподобных частиц гриппа после одновременной экспрессии только четырех структурных белков. J Virol. 2001. 75 (13): 6154–65.
CAS PubMed PubMed Central Статья Google ученый

Sailaja G, Skountzou I, Quan F-S, Compans RW, Kang S-M. Частицы вируса иммунодефицита человека активируют несколько типов иммунных клеток.Вирусология. 2007. 362 (2): 331–41.
CAS PubMed PubMed Central Статья Google ученый
Le DT, Radukic MT, Müller KM. Экспрессия капсидного белка аденоассоциированного вируса в Escherichia coli и химически определенная сборка капсида. Научные отчеты. 2019; 9 (1): 1–10.
Артикул CAS Google ученый
Джо С.К., Чаттерджи С., Ловреч Г., Адамс Т.Э., Тайсен-Андерсен М., Уолш Р. и др.Гликоинженерные частицы вируса гепатита B с повышенной иммуногенностью. Вакцина. 2020; 38 (22): 3892–901.
CAS PubMed Статья PubMed Central Google ученый
Чжай Л., Ядав Р., Кунда Н.К., Андерсон Д., Брукнер Э., Миллер Е.К. и др. Оральная иммунизация VLP бактериофага MS2-L2 защищает от инфекции полости рта и гениталий множественными типами ВПЧ, связанными с раком головы и шеи и раком шейки матки. Antiviral Res. 2019; 166: 56–65.
Antiviral Res. 2019; 166: 56–65.
CAS PubMed PubMed Central Статья Google ученый
Шири Ф., Петерсен К.Е., Романов В., Цзоу К., Гейл Б.К. Характеристика и дифференциальное удерживание вирусоподобных частиц бактериофага Q beta с использованием циклического электрического поля — фракционирования потока и асимметричного поля потока — фракционирования потока. Anal Bioanal Chem. 2020; 412 (7): 1563–72.
CAS PubMed Статья PubMed Central Google ученый
Mohsen MO, Gomes AC, Vogel M, Bachmann MF. Взаимодействие вирусоподобных частиц (VLP), происходящих из вирусного капсида, с врожденной иммунной системой. Вакцина. 2018; 6 (3): 37.
CAS PubMed Central Статья Google ученый
Силва А.Л., Перес С., Конниот Дж., Матос А.И., Моура Л., Каррейра Б. и др., Редакторы. Влияние наночастиц на рецепторы распознавания паттернов клеток врожденного иммунитета и активацию инфламмасом. Семинары по иммунологии; 2017: Эльзевир.
Влияние наночастиц на рецепторы распознавания паттернов клеток врожденного иммунитета и активацию инфламмасом. Семинары по иммунологии; 2017: Эльзевир.
Jeong H, Seong BL. Использование вирусоподобных частиц в качестве инновационных вакцин против возникающих вирусных инфекций. J Microbiol. 2017; 55 (3): 220–30.
CAS PubMed PubMed Central Статья Google ученый
Galaway FA, Stockley PG. Вирусоподобные частицы MS2: надежная полусинтетическая платформа для адресной доставки лекарств. Mol Pharm. 2013. 10 (1): 59–68.
CAS PubMed Статья PubMed Central Google ученый
Като Т, Юи М, Део ВК, Парк ЭЙ. Разработка вирусоподобных частиц саркомы Рауса, демонстрирующих hCC49 scFv для специфической адресной доставки лекарственного средства в клетки карциномы толстой кишки человека. Pharm Res. 2015; 32 (11): 3699–707.
CAS PubMed Статья PubMed Central Google ученый
Пан Х-Х, Чен П-И, Вэй К-Ц, Хуанг Ч. У, Шиуэ И-Л, Хуанг Ц-И и др. Доставка вирусоподобного нанотерапевтического агента с усилением конвекции с двухмодальной визуализацией для осаждения и искоренения опухолей головного мозга.Тераностика. 2019; 9 (6): 1752.
CAS PubMed PubMed Central Статья Google ученый
Garg A, Dewangan HK. Наночастицы как адъюванты в доставке вакцин. Critical Reviews ™ в терапевтических системах-носителях лекарственных средств. 2020; 37 (2).
Cimica V, Galarza JM. Составы адъювантов для вакцин на основе вирусоподобных частиц (VLP). Clin Immunol. 2017; 183: 99–108.
CAS PubMed PubMed Central Статья Google ученый
Дональдсон Б., Латиф З., Уокер Г.Ф., Янг С.Л., Уорд ВК. Вакцины с вирусоподобными частицами: иммунология и формулировка для клинического перевода. Экспертные ревакцины. 2018; 17 (9): 833–49.
CAS PubMed PubMed Central Статья Google ученый
Балке И., Зелтинс А. Использование вирусов растений и вирусоподобных частиц для создания новых вакцин. Adv Drug Deliv Rev.2019; 145: 119–29.
CAS PubMed Статья PubMed Central Google ученый
Ли Y-T, Ko E-J, Lee Y, Kim K-H, Kim M-C, Lee Y-N и др. Интраназальная вакцинация вирусоподобными частицами M2e5x вызывает гуморальные и клеточные иммунные ответы, обеспечивающие перекрестную защиту от гетероподтипных вирусов гриппа. PLoS ONE. 2018; 13 (1): e01
.PubMed PubMed Central Статья CAS Google ученый
Ван Ц., Чжэн Х, Гай В., Вонг Г, Ван Х, Джин Х и др. Новая вакцина с химерными вирусоподобными частицами, демонстрирующая домен, связывающий рецептор MERS-CoV, индуцирует специфический гуморальный и клеточный иммунный ответ у мышей.Antiviral Res. 2017; 140: 55–61.
CAS PubMed Статья PubMed Central Google ученый
D’Aoust MA, Couture MMJ, Charland N, Trepanier S, Landry N, Ors F и др. Производство вирусоподобных частиц на основе гемагглютинина в растениях: быстрый, эффективный и безопасный ответ на пандемический грипп. Plant Biotechnol J. 2010; 8 (5): 607–19.
PubMed Статья CAS PubMed Central Google ученый
Tregoning JS. Первое исследование эффективности вакцины против гриппа растительного происхождения на людях. Ланцет. 2020; 396 (10261): 1464–5.
CAS Статья Google ученый
Рокман С., Лори К.Л., Паркс С., Уитли А., Барр И.Г. Новые технологии противогриппозных вакцин. Микроорганизмы. 2020; 8 (11): 1745.
PubMed Central Статья Google ученый
Багливо С.Ю., Полоцк ФП.Долгий путь к защите младенцев от тяжелого заболевания нижних дыхательных путей, вызванного RSV. F1000 Исследования. 2019; 8.
Кич К., Альберт Дж., Чо И., Робертсон А., Рид П., Нил С. и др. Фаза 1-2 испытания вакцины на основе наночастиц рекомбинантного шипового белка SARS-CoV-2. N Engl J Med. 2020; 383 (24): 2320–32.
CAS PubMed Статья PubMed Central Google ученый
О’Доннелл К., Марци А. Гликопротеин вируса Эбола и его иммунные ответы на различных платформах вакцин.Экспертные ревакцины. 2020; 19 (3): 267–77.
PubMed Статья CAS PubMed Central Google ученый
Проффитт А. Первая одобренная вакцина против ВГЕ. Берлин: издательство Nature Publishing Group; 2012.
Книга Google ученый
Вебер Дж., Чейнсонг-Попов Р., Каллоу Д., Адамс С., Пату Дж., Ходжкин К. и др. Иммуногенность дрожжевых рекомбинантных вирусоподобных частиц p17p24: Ty (p24-VLP) у здоровых добровольцев.Вакцина. 1995. 13 (9): 831–4.
CAS PubMed Статья PubMed Central Google ученый
Атмар Р.Л., Бернштейн Д.И., Харро С.Д., Аль-Ибрагим М.С., Чен У.Х., Феррейра Дж. И др. Норовирусная вакцина против экспериментальной болезни, вызванной вирусом Норуолк. N Engl J Med. 2011; 365: 2178–87.
CAS PubMed PubMed Central Статья Google ученый
Chroboczek J, Szurgot I, Szolajska E.Вирусоподобные частицы в качестве вакцины. Acta Biochimica Polonica. 2014; 61 (3).
Chen XS, Casini G, Harrison SC, Garcea RL. Экспрессия капсидного белка вируса папилломы в Escherichia coli : очистка и сборка L1 HPV11 и HPV16. J Mol Biol. 2001. 307 (1): 173–82.
CAS PubMed Статья PubMed Central Google ученый
Salunke DM, Caspar DL, Garcea RL. Самосборка очищенного капсидного белка полиомавируса VP1.Клетка. 1986. 46 (6): 895–904.
CAS PubMed Статья PubMed Central Google ученый
Банди BC, Swartz JR. Эффективное образование дисульфидной связи в вирусоподобных частицах. J Biotechnol. 2011. 154 (4): 230–9.
CAS PubMed Статья PubMed Central Google ученый
Банди BC, Franciszkowicz MJ, Swartz JR. Бесклеточный синтез вирусоподобных частиц на основе Escherichia coli.Biotechnol Bioeng. 2008. 100 (1): 28–37.
CAS PubMed Статья PubMed Central Google ученый
Li H-Y, Han J-F, Qin C-F, Chen R. Вирусоподобные частицы для энтеровируса 71, полученные из Saccharomyces cerevisiae , сильно вызывают защитные иммунные ответы у мышей. Вакцина. 2013. 31 (32): 3281–7.
CAS PubMed Статья PubMed Central Google ученый
Родригес-Лимас, Вашингтон, Тио К.Э., Нильсен Дж., Рамирес О.Т., Паломарес, Лос-Анджелес. Молекулярный дизайн и процесс производства ротавирусоподобных частиц в Saccharomyces cerevisiae. Факт о микробной клетке. 2011; 10 (1): 1–10.
Артикул CAS Google ученый
Fernandes F, Teixeira AP, Carinhas N, Carrondo MJ, Alves PM. Клетки насекомых как производственная платформа сложных вирусоподобных частиц. Экспертные ревакцины. 2013. 12 (2): 225–36.
CAS PubMed Статья PubMed Central Google ученый
Скотти Н., Рыбицки Е.П. Вирусоподобные частицы, производимые в растениях в качестве потенциальных вакцин. Экспертные ревакцины. 2013; 12 (2): 211–24.
CAS PubMed Статья PubMed Central Google ученый
French T., Roy P. Синтез короподобных частиц вируса блютанга (BTV) рекомбинантным бакуловирусом, экспрессирующим два основных структурных коровых белка BTV. J Virol. 1990. 64 (4): 1530–6.
CAS PubMed PubMed Central Статья Google ученый
Chung Y-C, Ho M-S, Wu J-C, Chen W-J, Huang J-H, Chou S-T и др. Иммунизация вирусоподобными частицами энтеровируса 71 вызывает сильные иммунные ответы и защищает мышей от летального заражения. Вакцина. 2008. 26 (15): 1855–62.
CAS PubMed Статья PubMed Central Google ученый
Lin Y-L, Yu C-I, Hu Y-C, Tsai T-J, Kuo Y-C, Chi W-K, et al. Нейтрализующие антитела к энтеровирусу 71 типа в сыворотке макак, иммунизированных вирусоподобными частицами EV71.Вакцина. 2012. 30 (7): 1305–12.
CAS PubMed Статья PubMed Central Google ученый
Kibenge F, Qian B, Nagy E, Cleghorn J, Wadowska D. Образование вирусоподобных частиц, когда ген полипротеина (сегмент A) вируса инфекционной бурсальной болезни экспрессируется в клетках насекомых. Может J Vet Res. 1999; 63 (1): 49.
CAS PubMed PubMed Central Google ученый
Bräutigam S, Snezhkov E, Bishop DH. Образование полиовирусоподобных частиц рекомбинантными бакуловирусами, экспрессирующими отдельные белки VP0, VP3 и VP1, по сравнению с частицами, полученными из экспрессированного полипротеина полиовируса. Вирусология. 1993. 192 (2): 512–24.
PubMed Статья PubMed Central Google ученый
Vieira HL, Estêvão C, Roldão A, Peixoto CC, Sousa MF, Cruz PE, et al. Производство трехслойных ротавирусных ВПЧ: кинетика репликации вектора, стабильность мРНК и продукция рекомбинантного белка.J Biotechnol. 2005. 120 (1): 72–82.
CAS PubMed Статья PubMed Central Google ученый
Кирнбауэр Р., Тауб Дж., Гринстоун Х., Роден Р., Дюрст М., Гиссманн Л. и др. Эффективная самосборка L1 и L1 – L2 вируса папилломы человека типа 16 в вирусоподобные частицы. J Virol. 1993. 67 (12): 6929–36.
CAS PubMed PubMed Central Статья Google ученый
Злотник А., Мухопадхяй С. Сборка вирусов, аллостерия и противовирусные препараты. Trends Microbiol. 2011; 19 (1): 14–23.
CAS PubMed Статья PubMed Central Google ученый
Welsch S, Müller B, Kräusslich H-G. Более чем одна дверь — распространение вирусов в оболочке через клеточные мембраны. FEBS Lett. 2007. 581 (11): 2089–97.
CAS PubMed PubMed Central Статья Google ученый
Mortola E, Roy P. Эффективная сборка и высвобождение частиц, подобных коронавирусу SARS, с помощью гетерологичной системы экспрессии. FEBS Lett. 2004. 576 (1-2): 174–8.
CAS PubMed PubMed Central Статья Google ученый
Радд PM, Wormald MR, Stanfield RL, Huang M, Mattsson N, Speir JA, et al. Роль гликозилирования рецепторов клеточной поверхности, участвующих в распознавании клеточного иммунитета. J Mol Biol. 1999. 293 (2): 351–66.
CAS PubMed Статья PubMed Central Google ученый
Fontes-Garfias CR, Shan C, Luo H, Muruato AE, Medeiros DB, Mays E, et al. Функциональный анализ гликозилирования белка оболочки вируса Зика. Сотовые отчеты. 2017; 21 (5): 1180–90.
CAS PubMed PubMed Central Статья Google ученый
Bryant JE, Calvert AE, Mesesan K, Crabtree MB, Volpe KE, Silengo S, et al.Гликозилирование белка E вируса денге 2 по N67 имеет решающее значение для роста вируса in vitro, но не для роста комаров Aedes aegypti, инокулированных внутригрудно. Вирусология. 2007. 366 (2): 415–23.
CAS PubMed Статья PubMed Central Google ученый
Vicente T, Roldão A, Peixoto C, Carrondo MJ, Alves PM. Масштабное производство и очистка вакцин на основе VLP. J Invertebr Pathol. 2011; 107: S42–8.
CAS PubMed PubMed Central Статья Google ученый
Марсиан Дж., Фокс Х., Бахар М.В., Котеча А., Фрай Э., Стюарт Д.И. и др. Растительные стабилизированные VLP против полиомиелита типа 3 — кандидатная синтетическая вакцина против полиомиелита. Nat Commun. 2017; 8 (1): 1–9.
CAS Статья Google ученый
Chang G-JJ, Hunt AR, Holmes DA, Springfield T., Chiueh T.-S, Roehrig JT, et al.Усиление биосинтеза и секреции премембранных и оболочечных белков химерной плазмидой вируса денге 2 типа и вируса японского энцефалита. Вирусология. 2003. 306 (1): 170–80.
CAS PubMed Статья PubMed Central Google ученый
Zhang S, Liang M, Gu W, Li C, Miao F, Wang X и др. Вакцинация вирусоподобными частицами денге вызывает гуморальные и клеточные иммунные реакции у мышей. Вирол Дж. 2011; 8 (1): 1–9.
Артикул Google ученый
van Oers MM. Возможности и проблемы для системы экспрессии бакуловируса. J Invertebr Pathol. 2011; 107: S3–15.
PubMed Статья CAS PubMed Central Google ученый
Хиллебрандт Н., Вормиттаг П., Блатхардт Н., Дитрих А., Хаббух Дж. Интегрированный процесс улавливания и очистки вирусоподобных частиц: повышение производительности процесса за счет фильтрации с поперечным потоком.Фронт Bioeng Biotechnol. 2020; 8: 489.
PubMed PubMed Central Статья Google ученый
Peixoto C, Sousa M, Silva A, Carrondo M, Alves P. Последующая обработка трехслойных ротавирусоподобных частиц. J Biotechnol. 2007. 127 (3): 452–61.
CAS PubMed Статья PubMed Central Google ученый
Сёмин Б., Ильин Ю. Вирусоподобные частицы как инструмент производства вакцин.Mol Biol. 2019; 53 (3): 323–34.
CAS PubMed PubMed Central Статья Google ученый
Lünsdorf H, Gurramkonda C, Adnan A, Khanna N, Rinas U. Производство вирусоподобных частиц с помощью дрожжей: ультраструктурные и иммуноцитохимические исследования Pichia pastoris , производящего высокие уровни поверхностного антигена гепатита B. Факт о микробной клетке. 2011; 10 (1): 1–10.
Артикул CAS Google ученый
Сёмин Б., Пелиссон А., Ильин Ю.В., Бучетон А., ред. Экспрессия ретровируса gypsy Gag в культуре клеток Spodoptera frugiperda с рекомбинантным бакуловирусом. Доклады биохимии и биофизики; 2004: Springer.
Рен Дж., Белл Дж., Кой Д., Бруникарди Ф. Активация человеческого рецептора соматостатина типа 2 вызывает ингибирование роста клеток в трансфицированных HEK293, но не в трансфецированных клетках СНО. J Surg Res. 1997. 71 (1): 13–8.
CAS PubMed Статья PubMed Central Google ученый
Fuenmayor J, Gòdia F, Cervera L. Производство вирусоподобных частиц для вакцин. New Biotechnol. 2017; 39: 174–80.
CAS Статья Google ученый
Дональдсон Б., Аль-Барвани Ф., Янг В., Скаллион С., Уорд В., Янг С. Вирусоподобные частицы, универсальная платформа субъединичной вакцины. Доставка субъединичной вакцины. Берлин: Springer; 2015. с. 159–80.
Google ученый
Наскальска А., Пырч К. Вирусоподобные частицы как иммуногены и универсальные наноносители. Польский J Microbiol. 2015; 64 (1): 3–13.
Артикул Google ученый
Хуанг Х, Ван Х, Чжан Дж., Ся Н, Чжао К. Вирусоподобные частицы, полученные из Escherichia coli , при разработке вакцины. npj Vaccines. 2017; 2 (1): 1–9.
Артикул Google ученый
Hu Y, Huang S-J, Chu K, Wu T, Wang Z-Z, Yang C-L, et al.Безопасность бивалентного вируса папилломы человека, экспрессируемого Escherichia coli (типы 16 и 18), вакцины с вирусоподобными частицами L1: открытое клиническое испытание фазы I. Человеческие вакцины и иммунотерапевтические средства. 2014; 10 (2): 469–75.
Артикул Google ученый
Lacson E, Teng M, Ong J, Vienneau L, Ofsthun N, Lazarus JM. Антительный ответ на вакцинацию против гепатита B Engerix-B® и Recombivax-HB® при терминальной стадии почечной недостаточности. Hemodial Int.2005. 9 (4): 367–75.
PubMed Статья PubMed Central Google ученый
Nardin EH, Oliveira GA, Calvo-Calle JM, Wetzel K, Maier C, Birkett AJ, et al. Фаза I испытания вакцины против малярии, состоящей из ядерных частиц вируса гепатита В, экспрессирующих эпитопы циркумспорозоитов Plasmodium falciparum. Заражение иммунной. 2004. 72 (11): 6519–27.
CAS PubMed PubMed Central Статья Google ученый
Duffy PE, Патрик Горрес Дж. Вакцины против малярии с 2000 года: прогресс, приоритеты, продукты. npj Vaccines. 2020; 5 (48): 1–9.
Google ученый
Де Филетт М., Фирс В., Мартенс В., Биркетт А., Рамне А., Лёвенадлер Б. и др. Улучшенный дизайн и интраназальная доставка вакцины против гриппа человека на основе M2e. Вакцина. 2006. 24 (44–46): 6597–601.
PubMed Статья CAS PubMed Central Google ученый
Aires KA, Cianciarullo AM, Carneiro SM, Villa LL, Boccardo E, Pérez-Martinez G, et al. Получение вирусоподобных частиц L1 вируса папилломы человека типа 16 рекомбинантными клетками Lactobacillus casei . Appl Environ Microbiol. 2006. 72 (1): 745–52.
CAS PubMed PubMed Central Статья Google ученый
Фелпс Дж. П., Дао П., Джин Х., Расохова Л. Экспрессия и самосборка вирусоподобных частиц хлоротической пятнистости коровьего гороха в Pseudomonas fluorescens.J Biotechnol. 2007. 128 (2): 290–6.
CAS PubMed Статья PubMed Central Google ученый
Дай С., Ван Х., Дэн Ф. Достижения и проблемы в области вакцин на основе оболочечных вирусоподобных частиц (VLP). Журнал иммунологических наук. 2018; 2 (2).
Китинг Г.М., Ноубл С. Рекомбинантная вакцина против гепатита В (Engerix-B®). Наркотики. 2003. 63 (10): 1021–51.
CAS PubMed Статья PubMed Central Google ученый
Block SL, Nolan T, Sattler C, Barr E, Giacoletti KE, Marchant CD и др. Сравнение иммуногенности и реактогенности профилактической четырехвалентной вакцины против вируса папилломы человека (типы 6, 11, 16 и 18) L1 вирусоподобных частиц у подростков мужского и женского пола и молодых взрослых женщин. Педиатрия. 2006. 118 (5): 2135–45.
PubMed Статья PubMed Central Google ученый
Сарасват С., Атмарам Т, Парида М., Агарвал А, Саха А, Даш ПК.Экспрессия и характеристика дрожжевых частиц, подобных вирусу чикунгунья (CHIK-VLP), и их оценка в качестве потенциального кандидата на вакцину. PLoS Negl Trop Dis. 2016; 10 (7): e0004782.
PubMed PubMed Central Статья CAS Google ученый
Лю В., Цзян Х., Чжоу Дж., Ян Х, Тан И, Фанг Д. и др. Рекомбинантные вирусоподобные частицы денге из Pichia pastoris: эффективное продуцирование и иммунологические свойства.Гены вирусов. 2010. 40 (1): 53–9.
PubMed Статья CAS PubMed Central Google ученый
Баумерт Т.Ф., Ито С., Вонг Д.Т., Лян Т.Дж. Структурные белки вируса гепатита С собираются в вирусоподобные частицы в клетках насекомых. J Virol. 1998. 72 (5): 3827–36.
CAS PubMed PubMed Central Статья Google ученый
Wu C-Y, Yeh Y-C, Yang Y-C, Chou C, Liu M-T, Wu H-S, et al.Экспрессия вирусоподобных частиц млекопитающими для расширенной имитации подлинного вируса гриппа. PLoS ONE. 2010; 5 (3): e9784.
PubMed PubMed Central Статья CAS Google ученый
Чанг G-D, Чен C-J, Лин C-Y, Чен H-C, Чен Х. Улучшение гликозилирования в клетках насекомых с помощью гликозилтрансфераз млекопитающих. J Biotechnol. 2003. 102 (1): 61–71.
CAS Статья Google ученый
Глеба Ю., Климюк В., Мариллонне С. Магнифекция — новая платформа для экспрессии рекомбинантных вакцин в растениях. Вакцина. 2005. 23 (17–18): 2042–8.
CAS PubMed Статья PubMed Central Google ученый
Чарланд Н. Частицы, подобные вирусу гриппа растительного происхождения: для пандемии и не только. 2012.
Ширбагаи З., Болхассани А. Различные применения вирусоподобных частиц в биологии и медицине: вакцинация и системы доставки.Биополимеры. 2016; 105 (3): 113–32.
CAS PubMed Статья PubMed Central Google ученый
Харрисон Б., Уилсон Т. Основные этапы исследований вируса табачной мозаики. Philos Trans R Soc Lond B Biol Sci. 1999. 354 (1383): 521–9.
CAS PubMed PubMed Central Статья Google ученый
Goelet P, Lomonossoff G, Butler P, Akam M, Gait M, Karn J.Нуклеотидная последовательность РНК вируса табачной мозаики. Proc Natl Acad Sci. 1982. 79 (19): 5818–22.
CAS PubMed Статья PubMed Central Google ученый
Намба К., Стаббс Г. Структура вируса табачной мозаики при разрешении 3,6 A: значение для сборки. Наука. 1986. 231 (4744): 1401–6.
CAS PubMed Статья PubMed Central Google ученый
Рыбицкий Е.П. Молекулярное выращивание растений вирусоподобных наночастиц в качестве вакцин и реагентов. Wiley Interdiscipl Rev.2020; 12 (2): e1587.
Google ученый
Zhang T, Breitbart M, Lee WH, Run J-Q, Wei CL, Soh SWL, et al. Вирусное сообщество РНК в кале человека: преобладание патогенных вирусов растений. PLoS Biol. 2005; 4 (1): e3.
PubMed Central Статья CAS Google ученый
Wang C, Beiss V, Steinmetz NF. Наночастицы вируса мозаики коровьего гороха и пустые вирусоподобные частицы проявляют различные, но перекрывающиеся иммуностимулирующие свойства. Журнал вирусологии. 2019; 93 (21).
Балке И., Зелтинс А. Последние достижения в использовании растительных вирусоподобных частиц в качестве вакцин. Вирусы. 2020; 12 (3): 270.
CAS PubMed Central Статья Google ученый
Langeveld JP, Brennan FR, Martı́nez-Torrecuadrada JL, Jones TD, Boshuizen RS, Vela C, et al.Инактивированный рекомбинантный растительный вирус защищает собак от смертельного заражения парвовирусом собак. Вакцина. 2001. 19 (27): 3661–70.
CAS PubMed Статья PubMed Central Google ученый
Ян Си-Д, Ляо Дж-Т, Лай Си-Й, Чжон М.-Х, Лян С.-М., Линь И.-Л и др. Индукция защитного иммунитета у свиней рекомбинантным вирусом мозаики бамбука, экспрессирующим эпитопы вируса ящура. BMC Biotechnol. 2007; 7 (1): 1–11.
Артикул CAS Google ученый
Хуанг З., Чен К., Хьелм Б., Арнцен С., Мейсон Х. Система репликонов ДНК для быстрого высокоуровневого производства вирусоподобных частиц в растениях. Biotechnol Bioeng. 2009. 103 (4): 706–14.
CAS PubMed PubMed Central Статья Google ученый
Санти Л., Бэтчелор Л., Хуанг З., Хьельм Б., Килбурн Дж., Арнцен С.Дж. и др.Эффективная система экспрессии вируса растений, генерирующая орально иммуногенные вирусоподобные частицы Norwalk. Вакцина. 2008. 26 (15): 1846–54.
CAS PubMed PubMed Central Статья Google ученый
Деннис С.Дж., Мейерс А.Э., Гатри А.Дж., Хитцерот II, Рыбицки Е.П. Иммуногенность растительных вирусоподобных частиц африканской чумы лошадей: значение для новой вакцины. Plant Biotechnol J. 2018; 16 (2): 442–50.
CAS PubMed Статья PubMed Central Google ученый
Joung YH, Park SH, Moon K-B, Jeon J-H, Cho H-S, Kim H-S. Последние десять лет достижений в области рекомбинантных вакцин растительного происхождения против гепатита B. Int J Mol Sci. 2016; 17 (10): 1715.
PubMed Central Статья CAS Google ученый
Pniewski T, Kapusta J, Bocig P, Wojciechowicz J, Kostrzak A, Gdula M, et al. Оральная иммунизация низкими дозами лиофилизированной тканью устойчивого к гербицидам салата, экспрессирующей поверхностный антиген гепатита В, для прототипа таблетированной вакцины на основе растений.J Appl Genet. 2011. 52 (2): 125–36.
CAS PubMed Статья PubMed Central Google ученый
Чичестер Дж. А., Грин Б. Дж., Джонс Р. М., Шоджи Ю., Миура К., Лонг Калифорния и др. Безопасность и иммуногенность растительной вирусоподобной частицы Pfs25 в качестве вакцины против малярии, блокирующей передачу: исследование фазы 1 с увеличением дозы у здоровых взрослых. Вакцина. 2018; 36 (39): 5865–71.
CAS PubMed PubMed Central Статья Google ученый
Розалес-Мендоса С. Будут ли биофармацевтические препараты растительного происхождения играть роль в борьбе с COVID-19? Exp Opin Biol Ther. 2020; 20 (6): 545–8.
CAS Статья Google ученый
Purdy DE, Chang G-JJ. Секреция неинфекционных вирусоподобных частиц денге и идентификация аминокислот в области ствола, участвующих во внутриклеточном удержании белка оболочки. Вирусология. 2005. 333 (2): 239–50.
Li C, Liu F, Liang M, Zhang Q, Wang X, Wang T и др. Хантавирусоподобные частицы, генерируемые в клетках СНО, вызывают специфические иммунные ответы у мышей C57BL / 6. Вакцина. 2010. 28 (26): 4294–300.
CAS PubMed Статья PubMed Central Google ученый
Gutiérrez-Granados S, Cervera L, Mercedes Segura M, Wölfel J, Gòdia F. Оптимизированное производство вирусоподобных частиц ВИЧ-1 путем временной трансфекции в CAP-T-клетки.Прикладная микробиология и биотехнология. 2016; 100 (9): 3935–47.
PubMed Статья CAS PubMed Central Google ученый
Сюй Р., Ши М., Ли Дж., Сонг П., Ли Н. Конструирование вирусоподобных частиц SARS-CoV-2 с помощью системы экспрессии млекопитающих. Границы биоинженерии и биотехнологии. 2020; 8.
МакГиннес Л.В., Гравий К.А., Финберг Р.В., Курт-Джонс Э.А., Массар М.Дж., Смит Дж. И др. Сборка и иммунологические свойства вирусоподобных частиц болезни Ньюкасла, содержащих белки F и G респираторно-синцитиального вируса.J Virol. 2011; 85 (1): 366–77.
CAS PubMed Статья PubMed Central Google ученый
Glass PJ, White LJ, Ball JM, Leparc-Goffart I, Hardy ME, Estes MK. Открытая рамка считывания 3 вируса Norwalk кодирует минорный структурный белок. J Virol. 2000. 74 (14): 6581–91.
CAS PubMed PubMed Central Статья Google ученый
Lai C-C, Cheng Y-C, Chen P-W, Lin T-H, Tzeng T-T, Lu C-C, et al.Разработка процесса производства вакцины VLP против пандемического гриппа с использованием системы экспрессии бакуловируса. J Biol Eng. 2019; 13 (1): 1–9.
CAS Статья Google ученый
Хатчинс Б., Саджади Н., Сивер С., Шеперд А., Бауэр С. Р., Симек С. и др. Работа над стандартом тестирования аденовирусных векторов. Mol Ther. 2000. 2 (6): 532–4.
CAS PubMed Статья PubMed Central Google ученый
Луа Л.Х., Коннорс Н.К., Сейнсбери Ф., Чуан Ю.П., Вибово Н., Мидделберг А.П. Биоинженерия вирусоподобных частиц в качестве вакцин. Biotechnol Bioeng. 2014. 111 (3): 425–40.
CAS PubMed Статья PubMed Central Google ученый
Мартинс К.А., Купер С.Л., Стронски С.М., Норрис С.Л., Квилас С.А., Стеффенс Дж. Т. и др. Т-клеточные ответы CD4, усиленные адъювантом, имеют решающее значение для стойкого иммунитета к вакцинам. EBioMedicine. 2016; 3: 67–78.
PubMed Статья PubMed Central Google ученый
Темизоз Б, Курода Э, Исии К.Дж. Адъюванты вакцин как потенциальные иммунотерапевтические средства против рака. Int Immunol. 2016; 28 (7): 329–38.
CAS PubMed PubMed Central Статья Google ученый
Лопес О., Оливейра М., Гарсия Е.А., Квон Б.Дж., Достер А., Осорио Ф.А. Защита от инфицирования вирусом репродуктивного и респираторного синдрома свиней (PRRSV) посредством пассивного переноса нейтрализующих PRRSV антител зависит от дозы.Clin Vaccine Immunol. 2007. 14 (3): 269–75.
CAS PubMed PubMed Central Статья Google ученый
Galarza JM, Latham T, Cupo A. Вакцина с вирусоподобными частицами (VLP) обеспечивала полную защиту от заражения вирусом летального гриппа. Viral Immunol. 2005. 18 (1): 244–51.
CAS PubMed Статья PubMed Central Google ученый
Quan F-S, Ko E-J, Kwon Y-M, Joo KH, Compans RW, Kang S-M. Адъюванты слизистой оболочки для вакцины с вирусоподобными частицами гриппа. Viral Immunol. 2013. 26 (6): 385–95.
CAS PubMed PubMed Central Статья Google ученый
Thiam F, Charpilienne A, Poncet D, Kohli E, Basset C. Субъединицы B холерного токсина и термолабильный энтеротоксин Escherichia coli обладают таким же адъювантным действием, как и целые молекулы, на ответы антител, специфичных для ротавирусов 2/6-VLP, и вызвать Th27-подобный ответ после интраректальной иммунизации.Microb Pathog. 2015; 89: 27–34.
CAS PubMed Статья PubMed Central Google ученый
Гу И, Вэй М., Ван Д, Ли З, Се М., Пан Х и др. Характеристика бивалентной вакцины от вируса папилломы человека типа 16 и 18, производного от Escherichia coli. Вакцина. 2017; 35 (35): 4637–45.
CAS PubMed Статья PubMed Central Google ученый
Шарма В.К., Шарма И., Глик Дж. Возрастающая роль масс-спектрометрии в области разработки вакцин. Масс-спектром. Rev.2020; 39 (1-2): 83-104.
CAS PubMed Статья PubMed Central Google ученый
Yang Y, Li H, Li Z, Zhang Y, Zhang S, Chen Y, Su Z. ВЭЖХ с исключением размера обеспечивает простой, быстрый и универсальный альтернативный метод контроля качества вакцин путем определения характеристик сборки антигенов.Вакцина. 2015; 33 (9): 1143–50.
CAS PubMed Статья PubMed Central Google ученый
Шитухина А., Пристацкий П., Хе Дж., Казимиро Д.Р., Шварц Р.М., Хоанг В.М. и др. Разработка и применение метода высокоэффективной жидкостной хроматографии с обращенной фазой для количественного определения и характеристики вакцины с вирусоподобными частицами чикунгунья. J Chromatogr A. 2014; 1364: 192–7.
CAS PubMed PubMed Central Статья Google ученый
Li TC, Takeda N, Kato K, Nilsson J, Xing L, Haag L, Cheng RH, Miyamura T. Характеристика самособирающихся вирусоподобных частиц человеческого полиомавируса BK, генерируемых рекомбинантными бакуловирусами. Вирусология. 2003. 311 (1): 115–24.
CAS PubMed Статья PubMed Central Google ученый
Оропеса Р., Рамос Дж. Р., Фалькон В., Фелипе А. Характеристика вирусоподобных частиц с помощью атомно-силовой микроскопии в условиях окружающей среды.Adv Nat Sci. 2013; 4 (2): 025007.
Google ученый
Zhao Q, Allen MJ, Wang Y, Wang B, Wang N, Shi L, et al. Разборка и повторная сборка улучшает морфологию и термическую стабильность вирусоподобных частиц вируса папилломы человека 16 типа. Наномедицина. 2012; 8 (7): 1182–9.
CAS PubMed Статья PubMed Central Google ученый
Чуан Ю.П., Фан YY, Луа Л., Мидделберг А.П.Количественный анализ размера и распределения вирусоподобных частиц путем фракционирования в полевом потоке. Biotechnol Bioeng. 2008. 99 (6): 1425–33.
CAS PubMed Статья PubMed Central Google ученый
Pease LF III, Lipin DI, Tsai DH, Zachariah MR, Lua LH, Tarlov MJ, et al. Количественная характеристика вирусоподобных частиц с помощью асимметричного фракционирования потока в поле потока, анализа дифференциальной подвижности с электрораспылением и просвечивающей электронной микроскопии.Biotechnol Bioeng. 2009. 102 (3): 845–55.
CAS PubMed Статья PubMed Central Google ученый
Zhang X, Wei M, Pan H, Lin Z, Wang K, Weng Z, et al. Надежное производство и всесторонняя характеристика рекомбинантных вирусоподобных частиц гепатита Е в Hecolin®. Вакцина. 2014. 32 (32): 4039–50.
CAS PubMed Статья PubMed Central Google ученый
Зелтинс А. Конструирование и характеристика вирусоподобных частиц: обзор. Mol Biotechnol. 2013. 53 (1): 92–107.
CAS PubMed Статья PubMed Central Google ученый
Yang Y, Su Z, Ma G, Zhang S. Определение характеристик и стабилизация процесса разработки и рецептуры продукта для сверхбольших белковых частиц. Eng Life Sci. 2020; 20 (11): 451–65.
PubMed PubMed Central Статья CAS Google ученый
Zhao Q, Modis Y, High K, Towne V, Meng Y, Wang Y, et al. Разборка и повторная сборка вирусоподобных частиц вируса папилломы человека приводит к большей реактивности вирионоподобных антител. Virology J. 2012; 9 (1): 1–14.
Артикул CAS Google ученый
Splawn L, Bailey C, Medina J, Cho JC. Вакцинация Heplisav-B для профилактики заражения вирусом гепатита B у взрослых в США. Наркотики сегодня. 2018; 54 (7): 399–405.
CAS Статья Google ученый
Неттер Х. Дж., Чанг С. Ф., Брунс М. Диапазон хозяев и патогенность вирусов гепатита В. 2008.
Qian C, Liu X, Xu Q, Wang Z, Chen J, Li T, et al. Недавний прогресс в универсальности вирусоподобных частиц. Вакцина. 2020; 8 (1): 139.
CAS PubMed Central Статья Google ученый
Wei M, Wang D, Li Z, Song S, Kong X, Mo X и др. Укорочение N-конца на белках L1 вирусов папилломы человека способствует их растворимой экспрессии в Escherichia coli и самосборке in vitro. Новые микробы и инфекции. 2018; 7 (1): 1–12.
Google ученый
Кондо К. Разработка вакцины против ВПЧ — нерешенные вопросы и перспективы. Нихон Риншо Jpn J Clin Med. 2009. 67 (1): 62–8.
Google ученый
Mohsen MO, Zha L, Cabral-Miranda G, Bachmann MF, редакторы. Основные открытия и последние достижения в области вакцин на основе вирусоподобных частиц (VLP). Семинары по иммунологии; 2017: Эльзевир.
Li Z, Wang D, Gu Y, Song S, He M, Shi J, et al. Кристаллические структуры двух иммунных комплексов определяют детерминанты вирусной инфекционности и типоспецифической нейтрализации вируса папилломы человека. MBio. 2017; 8 (5).
Беран Дж. Безопасность и иммуногенность новой вакцины против гепатита В для защиты пациентов с почечной недостаточностью, включая пациентов, находящихся на предварительном гемодиализе и гемодиализе.Экспертное мнение Biol Ther. 2008. 8 (2): 235–47.
CAS PubMed Статья PubMed Central Google ученый
Deschuyteneer M, Elouahabi A, Plainchamp D, Plisnier M, Soete D, Corazza Y, et al. Молекулярная и структурная характеристика вирусоподобных частиц L1, которые используются в качестве вакцинных антигенов в Cervarix, вакцине против рака шейки матки с адъювантом AS04 против ВПЧ-16 и -18. Человеческие вакцины. 2010. 6 (5): 407–19.
CAS PubMed Статья PubMed Central Google ученый
Wu T, Li S-W, Zhang J, Ng M-H, Xia N-S, Zhao Q. Разработка вакцины против гепатита E: 14-летняя одиссея. Hum Vaccines Immunother. 2012; 8 (6): 823–7.
CAS Статья Google ученый
Цай В., Тан З-М, Вэнь Г.-П, Ван С.-Л., Джи В.-Ф, Ян М. и др. Высокопроизводительный нейтрализующий анализ на антитела и сыворотки против вируса гепатита E. Научные отчеты. 2016; 6 (1): 1–8.
CAS Статья Google ученый
Li SW, Zhang J, Li YM, Ou SH, Huang GY, He ZQ и др. Вакцина против гепатита Е с бактериальной экспрессией: антигенность, иммуногенность и защитная способность на приматах. Вакцина. 2005. 23 (22): 2893–901.
CAS PubMed Статья PubMed Central Google ученый
Zhu F-C, Zhang J, Zhang X-F, Zhou C, Wang Z-Z, Huang S-J, et al. Эффективность и безопасность рекомбинантной вакцины против гепатита Е у здоровых взрослых: крупномасштабное рандомизированное двойное слепое плацебо-контролируемое исследование фазы 3.Ланцет. 2010. 376 (9744): 895–902.
CAS PubMed Статья PubMed Central Google ученый
Yuen CY, Dodgson JE, Tarrant M. Восприятие гонконгских китайских женщин относительно вакцинации против гриппа во время беременности. Вакцина. 2016; 34 (1): 33–40.
PubMed Статья PubMed Central Google ученый
Марсиан Дж., Ломоносов Г.П. Молекулярный фарминг — VLP, производимые в растениях.Curr Opin Biotechnol. 2016; 37: 201–6.
CAS PubMed Статья PubMed Central Google ученый
Доан Л.Х., Ли М., Чен С., Яо К. Вирусоподобные частицы в качестве вакцин против ВИЧ-1. Rev Med Virol. 2005. 15 (2): 75–88.
PubMed Статья PubMed Central Google ученый
Пульчини С., Массин С., Лаунай О., Верже П. Факторы, связанные с вакцинацией против гепатита В, коклюша, сезонного и пандемического гриппа среди французских врачей общей практики: исследование 2010 года.Вакцина. 2013. 31 (37): 3943–9.
PubMed Статья PubMed Central Google ученый
Гавликова С., Личкова М., Клемпа Б. Невиремическая передача клещевых вирусов. Acta Virol. 2013; 57 (2): 123–9.
CAS PubMed Статья PubMed Central Google ученый
Хербст-Краловец М., Мейсон Х.С., Чен К. Норуолкские вирусоподобные частицы в качестве вакцин.Экспертные ревакцины. 2010. 9 (3): 299–307.
CAS PubMed PubMed Central Статья Google ученый
Олдстоун М. Аренавирусы I-Эпидемиология, молекулярная и клеточная биология аренавирусов-Предисловие. Аренавирусы. 2002; 262: 5–12.
Google ученый
Бранко Л.М., Гроув Дж. Н., Геске Ф.Дж., Бойзен М.Л., Манси И.Дж., Мальято С.А. и др. Вирусоподобные частицы Ласса, отображающие все основные иммунологические детерминанты, в качестве кандидата на вакцину от геморрагической лихорадки Ласса.Вирол Дж. 2010; 7 (1): 1–19.
Артикул CAS Google ученый
Zhou Z, Wang M-I, Deng F, Li T, Hu Z, Wang H-I. Производство вирусоподобных частиц CCHF системой экспрессии бакуловирусных клеток-насекомых. Virologica Sinica. 2011; 26 (5): 338–46.
CAS PubMed PubMed Central Статья Google ученый
Warfield KL, Posten NA, Swenson DL, Olinger GG, Esposito D, Gillette WK, et al.Филовирусоподобные частицы, продуцируемые в клетках насекомых: иммуногенность и защита у грызунов. Журнал инфекционных болезней. 2007; 196 (Приложение_2): S421-S9.
Варфилд К.Л., Босио С.М., Велчер Б.К., Дил Э.М., Мохамадзаде М., Шмальджон А. и др. Частицы, похожие на вирус Эбола, защищают от смертельной инфекции вирусом Эбола. Proc Natl Acad Sci. 2003. 100 (26): 15889–94.
CAS PubMed Статья PubMed Central Google ученый
Уолпита П., Барр Дж., Шерман М., Баслер К.Ф., Ван Л. Вакцинный потенциал вирусоподобных частиц Нипах. PLoS ONE. 2011; 6 (4): e18437.
CAS PubMed PubMed Central Статья Google ученый
Kong D, Wen Z, Su H, Ge J, Chen W, Wang X и др. Вакцины против энцефалита нипахского энцефалита, переносимые вирусом ньюкаслской болезни, вызывают у мышей В- и Т-клеточные ответы, а у свиней — нейтрализующие антитела длительного действия. Вирусология. 2012. 432 (2): 327–35.
CAS PubMed Статья PubMed Central Google ученый
Zabel F, Kündig TM, Bachmann MF. Гуморальный иммунитет, индуцированный вирусами: как инициируются В-клеточные реакции. Curr Opin Virol. 2013. 3 (3): 357–62.
CAS PubMed Статья PubMed Central Google ученый
Линк А, Забель Ф, Шнетцлер Й, Титц А, Бромбахер Ф, Бахманн МФ.Врожденный иммунитет опосредует фолликулярный транспорт твердого, но не растворимого белкового антигена. J Immunol. 2012. 188 (8): 3724–33.
CAS PubMed Статья PubMed Central Google ученый
Манолова В., Флас А, Бауэр М., Шварц К., Саудан П., Бахманн М.Ф. Наночастицы нацелены на различные популяции дендритных клеток в зависимости от их размера. Eur J Immunol. 2008. 38 (5): 1404–13.
CAS PubMed Статья PubMed Central Google ученый
Аль-Барвани Ф, Янг С.Л., Бэрд М.А., Ларсен Д.С., Уорд В.К. Маннозилирование вирусоподобных частиц усиливает интернализацию антигенпрезентирующими клетками. PLoS ONE. 2014; 9 (8): e104523.
PubMed PubMed Central Статья CAS Google ученый
Win SJ, Ward VK, Dunbar PR, Young SL, Baird MA. Перекрестное представление эпитопов на вирусоподобных частицах посредством пути рециклинга рецептора MHC I. Immunol Cell Biol. 2011. 89 (6): 681–8.
CAS PubMed Статья PubMed Central Google ученый
Буонагуро Л., Торнеселло М., Тальямонте М., Галло Р., Ван Л., Камин-Льюис Р. и др. Полученные из бакуловируса вирусоподобные частицы вируса иммунодефицита человека типа 1 активируют дендритные клетки и индуцируют Т-клеточные ответы ex vivo. J Virol. 2006. 80 (18): 9134–43.
CAS PubMed PubMed Central Статья Google ученый
Bournazos S, Wang TT, Ravetch JV. Роль и функция рецепторов Fcγ на миелоидных клетках. Миелоидные клетки в здоровье и болезни: синтез. 2017: 405–27.
Fiebiger E, Meraner P, Weber E, Fang I-F, Stingl G, Ploegh H, et al. Цитокины регулируют протеолиз в главном комплексе гистосовместимости класса II — зависимой презентации антигена дендритными клетками. J Exp Med. 2001. 193 (8): 881–92.
CAS PubMed PubMed Central Статья Google ученый
Sallusto F, Lanzavecchia A. Понимание движения дендритных клеток и Т-лимфоцитов посредством анализа экспрессии хемокиновых рецепторов. Immunol Rev.2000; 177: 134–40.
CAS PubMed Статья PubMed Central Google ученый
Деринг М., Близ Х., Коллер Н., Тишер-Циммерманн С., Мюскен М., Хенрих Ф. и др. Модуляция TAP-зависимой компартментализации антигена во время дифференцировки моноцитов человека в DC.Blood Adv. 2019; 3 (6): 839–50.
PubMed PubMed Central Статья CAS Google ученый
Лангенкамп А., Месси М., Ланзавеккья А., Саллусто Ф. Кинетика активации дендритных клеток: влияние на прайминг TH 1, TH 2 и неполяризованных Т-клеток. Nat Immunol. 2000. 1 (4): 311–6.
CAS PubMed Статья PubMed Central Google ученый
Banchereau J, Steinman RM. Дендритные клетки и контроль иммунитета. Природа. 1998. 392 (6673): 245–52.
CAS PubMed Статья PubMed Central Google ученый
Кин Дж., Форман Дж. Хелперная активность необходима для образования цитотоксических Т-лимфоцитов in vivo. J Exp Med. 1982; 155 (3): 768–82.
CAS PubMed PubMed Central Статья Google ученый
Паркер, округ Колумбия. Т-клеточно-зависимая активация В-клеток. Анну Рев Иммунол. 1993. 11 (1): 331–60.
CAS PubMed Статья PubMed Central Google ученый
Морон В.Г., Руэда П., Седлик С., Леклерк С. In vivo дендритные клетки могут перекрестно представлять вирусоподобные частицы, используя путь от эндосомы к цитозолю. J Immunol. 2003. 171 (5): 2242–50.
PubMed Статья PubMed Central Google ученый
Бесса Дж., Забель Ф., Линк А, Егерленер А., Хинтон Х. Дж., Шмитц Н. и др. В-клетки с низким сродством переносят вирусные частицы из легких в селезенку, чтобы инициировать ответы антител. Proc Natl Acad Sci. 2012. 109 (50): 20566–71.
CAS PubMed Статья PubMed Central Google ученый
Лопес-Масиас С. Вакцины против пандемического гриппа на основе вирусоподобных частиц (VLP): эффективность вакцины VLP во время пандемии гриппа 2009 года.Hum Vaccines Immunother. 2012; 8 (3): 411–4.
Артикул CAS Google ученый
Яо К., Чжан Р., Го Л., Ли М., Чен С. Независимые от Th-клеток иммунные ответы на вакцину с химерным гемагглютинином / обезьяньим вирусом иммунодефицита человека с частицами вакцины. J Immunol. 2004. 173 (3): 1951–1958.
CAS PubMed Статья PubMed Central Google ученый
Lenz P, Lowy DR, Schiller JT.Вирусоподобные частицы папилломавируса индуцируют цитокины, характерные для врожденных иммунных ответов в плазматических дендритных клетках. Eur J Immunol. 2005. 35 (5): 1548–56.
CAS PubMed Статья PubMed Central Google ученый
Сонг Дж. М., Ван Би З., Пак К. М., Ван Ройен Н., Куан Ф. С., Ким М. К. и др. Вирусоподобные частицы гриппа, содержащие М2, вызывают широкий перекрестный защитный иммунитет. PLoS ONE. 2011; 6 (1): e14538.
CAS PubMed PubMed Central Статья Google ученый
Росс Т.М., Махмуд К., Кварар С.Дж., Шнайдер-Охрум К., Хитон П.М., Брайт Р.А. Вакцина из трехвалентных вирусоподобных частиц вызывает защитный иммунный ответ против сезонных штаммов гриппа у мышей и хорьков. PLoS ONE. 2009; 4 (6): e6032.
PubMed PubMed Central Статья CAS Google ученый
Serradell MC, Rupil LL, Martino RA, Prucca CG, Carranza PG, Saura A, et al. Эффективная оральная вакцинация с помощью биоинженерных вирусоподобных частиц с поверхностными белками простейших. Nat Commun. 2019; 10 (1): 1–15.
Артикул CAS Google ученый
Гуо Дж., Чжоу А., Сунь Х, Ша В, Ай К., Пан Дж. И др. Иммуногенность вакцины на основе вирусоподобных частиц, содержащей несколько антигенных эпитопов toxoplasma gondii, против острого и хронического токсоплазмоза у мышей.Фронт Иммунол. 2019; 10: 592.
CAS PubMed PubMed Central Статья Google ученый
Heath WR, Carbone FR. Перекрестная презентация вирусного иммунитета и самотолерантности. Nat Rev Immunol. 2001. 1 (2): 126–34.
CAS PubMed Статья PubMed Central Google ученый
Джейнвей К.А., Капра Дж. Д., Трэверс П., Уолпорт М. Иммунобиология: иммунная система в здоровье и болезнях, 1999.
Руэдл С., Сторни Т., Лехнер Ф., Бечи Т., Бахманн М.Ф. Перекрестная презентация вирусоподобных частиц CD8-дендритными клетками кожи: незаменимая роль TAP. Eur J Immunol. 2002. 32 (3): 818–25.
CAS PubMed Статья PubMed Central Google ученый
Mandell RB, Koukuntla R, Mogler LJ, Carzoli AK, Freiberg AN, Holbrook MR, et al. Вакцина против лихорадки Рифт-Валли, не способная к репликации: химерные вирусоподобные частицы защищают мышей и крыс от смертельного заражения.Вирусология. 2010. 397 (1): 187–98.
CAS PubMed Статья PubMed Central Google ученый
Munoz N, Bosch FX, Castellsagué X, Díaz M, De Sanjose S, Hammouda D, et al. Против каких типов вируса папилломы человека мы должны проводить вакцинацию и скрининг? Международная перспектива. Int J Cancer. 2004. 111 (2): 278–85.
CAS PubMed Статья PubMed Central Google ученый
Смит Дж. С., Линдси Л., Хутс Б., Киз Дж., Франчески С., Винер Р. и др. Распределение типа вируса папилломы человека при инвазивном раке шейки матки и поражениях шейки матки высокой степени: обновление метаанализа. Int J Cancer. 2007. 121 (3): 621–32.
CAS PubMed Статья PubMed Central Google ученый
Yim E-K, Park J-S. Роль онкопротеинов Е6 и Е7 ВПЧ в канцерогенезе шейки матки, ассоциированном с ВПЧ. Лечение рака Res.2005; 37 (6): 319.
PubMed PubMed Central Статья Google ученый
Huibregtse JM, Scheffner M, редакторы. Механизмы инактивации опухолевых супрессорных белков онкобелками Е6 и Е7 вируса папилломы человека. Семинары по ВИРОЛОГИИ; 1994: Эльзевир.
Zhang T, Chen X, Liu H, Bao Q, Wang Z, Liao G и др. Рационально разработанный слитый белок флагеллин-L2 индуцировал нейтрализующие антитела в сыворотке и слизистой оболочке против нескольких типов HPV.Вакцина. 2019; 37 (30): 4022–30.
CAS PubMed Статья PubMed Central Google ученый
Пуянфард С., Спаньоли Дж., Булли Л., Бальц К., Ян Ф., Оденвальд С. и др. Политоп второстепенного капсидного белка L2 индуцирует широкую защиту от онкогенных вирусов папилломы человека и слизистых оболочек. Журнал вирусологии. 2018; 92 (4).
Ядав Р., Чжай Л., Тумбан Э. Вакцины L2 на основе вирусоподобных частиц против ВПЧ: где мы находимся сегодня? Вирусы.2020; 12 (1): 18.
CAS Статья Google ученый
Zhai L, Peabody J, Pang YS, Schiller J, Chackerian B, Tumban E. Новый кандидат в вакцину против ВПЧ: VLP фага MS2, демонстрирующий тандемный пептид L2 ВПЧ, обеспечивает защиту мышей, аналогичную Гардасилу-9. Antivir Res. 2017; 147: 116–23.
CAS PubMed Статья PubMed Central Google ученый
Janitzek CM, Peabody J, Thrane S, Carlsen PH, Theander TG, Salanti A, et al. Доказательство концепции разработки комбинаторной вакцины против ВПЧ и плацентарной малярии на основе VLP. Научный доклад 2019; 9 (1): 1–10.
CAS Статья Google ученый
Сламон Д.Д., Кларк Г.М., Вонг С.Г., Левин В.Дж., Ульрих А., Макгуайр В.Л. Рак груди человека: корреляция рецидива и выживаемости с амплификацией онкогена HER-2 / neu. Наука.1987. 235 (4785): 177–82.
CAS PubMed Статья PubMed Central Google ученый
Бьянкини Г., Джанни Л. Иммунная система и ответ на лечение, направленное на HER2, при раке молочной железы. Ланцет Онкол. 2014; 15 (2): e58–68.
CAS PubMed Статья PubMed Central Google ученый
Гарг А., Куартино А., Ли Дж., Джин Дж., Вада Д. Р., Ли Х и др.Популяционный фармакокинетический и ковариативный анализ пертузумаба, моноклонального антитела, нацеленного на HER2, и оценка фиксированной дозы, не зависящей от веса, у пациентов с различными солидными опухолями. Cancer Chemother Pharmacol. 2014; 74 (4): 819–29.
CAS PubMed Статья PubMed Central Google ученый
Лейланд-Джонс Б. График дозирования — Герцептин®. Онкология. 2001; 61 (Приложение 2): 31–6.
CAS PubMed Статья PubMed Central Google ученый
Палладини А., Трейн С., Яницек С.М., Пил Дж., Клемменсен С.Б., де Йонг В.А. и др. Отображение HER2 вирусоподобными частицами вызывает сильные противораковые реакции. Онкоиммунология. 2018; 7 (3): e1408749.
PubMed PubMed Central Статья Google ученый
Конти Л., Болли Е., Ди Лоренцо А., Франчески В., Макки Ф., Риккардо Ф. и др. Иммунное нацеливание на цистин / глутаматный антипортер xCT усиливает эффективность нацеленных на Her2 иммунотерапевтических средств при раке молочной железы.Cance Immunol Res. 2020; 8 (8): 1039–53.
CAS Статья Google ученый
Rolih V, Caldeira J, Bolli E, Salameh A, Conti L., Barutello G, et al. Разработка вакцины на основе vlp с внеклеточным доменом XCT для лечения метастатического рака молочной железы. Раки. 2020; 12 (6): 1492.
CAS PubMed Central Статья Google ученый
Bolli E, O’Rourke JP, Conti L, Lanzardo S, Rolih V, Christen JM и др. Иммунотерапия вирусоподобными частицами, нацеленная на эпитоп-специфический анти-xCT, экспрессируемый на раковых стволовых клетках, ингибирует прогрессирование метастатического рака in vivo. Онкоиммунология. 2018; 7 (3): e1408746.
PubMed Статья PubMed Central Google ученый
Zhang S, Yong LK, Li D, Cubas R, Chen C, Yao Q. Иммунизация мезотелин-вирусоподобными частицами контролирует рост рака поджелудочной железы посредством индукции CD8 + Т-клеток и снижения частоты регуляции CD4 + foxp3 + ICOS- Т-клетки.PLoS ONE. 2013; 8 (7): e68303.
CAS PubMed PubMed Central Статья Google ученый
Фонг Д., Мозер П., Краммель С., Гостнер Дж., Маргрейтер Р., Миттерер М. и др. Высокая экспрессия TROP2 коррелирует с плохим прогнозом рака поджелудочной железы. Br J Рак. 2008. 99 (8): 1290–5.
CAS PubMed PubMed Central Статья Google ученый
Кубас Р., Чжан С., Ли М., Чен С., Яо К. Химерные вирусоподобные частицы Trop2: потенциальный иммунотерапевтический подход против рака поджелудочной железы. J Immunother. 2011. 34 (3): 251–63.
CAS PubMed Статья PubMed Central Google ученый
Брей Ф., Ферли Дж., Сурджоматарам И., Сигель Р.Л., Торре Л.А., Джемаль А. Глобальная статистика рака 2018: оценки GLOBOCAN заболеваемости и смертности от 36 раковых заболеваний в 185 странах во всем мире.Рак J Clin. 2018; 68 (6): 394–424.
Артикул Google ученый
Лизотт П., Вен А., Шин М., Филдс Дж., Роджанасопондист П., Стейнмец Н. и др. Вакцинация in situ наночастицами вируса мозаики вигны подавляет метастатический рак. Nat Nanotechnol. 2016; 11 (3): 295–303.
CAS PubMed Статья PubMed Central Google ученый
Mohsen MO, Vogel M, Riether C., Muller J, Salatino S, Ternette N, et al.Нацеливание на мутированные и зародышевые эпитопы обеспечивает доклиническую эффективность мгновенно созданной противораковой нановакцины. Фронт Иммунол. 2019; 10: 1015.
CAS PubMed PubMed Central Статья Google ученый
Mohsen MO, Heath MD, Cabral-Miranda G, Lipp C, Zeltins A, Sande M, et al. Вакцинация наночастицами в сочетании с микроадъювантами защищает от рака. J Immunother Cancer. 2019; 7 (1): 1–12.
Артикул Google ученый
Zdanowicz M, Chroboczek J. Вирусоподобные частицы как векторы доставки лекарств. Acta Biochim Pol. 2016; 63 (3): 469–73.
CAS PubMed Статья PubMed Central Google ученый
Zochowska M, Paca A, Schoehn G, Andrieu J-P, Chroboczek J, Dublet B, et al. Додекаэдр аденовируса как вектор доставки лекарств. PLoS ONE. 2009; 4 (5): e5569.
PubMed PubMed Central Статья CAS Google ученый
Shan L, Cui S, Du C, Wan S, Qian Z, Achilefu S, et al. Аденовирусный вектор, конъюгированный с паклитакселом, для направленной доставки лекарств для лечения опухолей. Биоматериалы. 2012. 33 (1): 146–62.
CAS PubMed Статья PubMed Central Google ученый
Зоховска М., Пигуэт А.С., Джемиелити Дж., Ковальска Дж., Шолайска Е., Дюфур Дж. Ф. и др. Опосредуемая вирусоподобными частицами внутриклеточная доставка аналога кэпа мРНК с активностью in vivo против гепатоцеллюлярной карциномы.Наномедицина. 2015; 11 (1): 67–76.
CAS PubMed Статья PubMed Central Google ученый
Эшли К.Э., Карнес Е.С., Филлипс Г.К., Дерфи П.Н., Були М.Д., Лино Калифорния и др. Клеточно-специфическая доставка различных грузов вирусоподобными частицами бактериофага MS2. САУ Нано. 2011. 5 (7): 5729–45.
CAS PubMed PubMed Central Статья Google ученый
Чжао К., Чен В., Чен Ю., Чжан Л., Чжан Дж., Чжан З. Самособирающиеся вирусоподобные частицы из структурного белка ротавируса VP6 для адресной доставки лекарств. Bioconjug Chem. 2011; 22 (3): 346–52.
CAS PubMed Статья PubMed Central Google ученый
Aljabali AA, Shukla S, Lomonossoff GP, Steinmetz NF, Evans DJ. Cpmv-dox доставляет. Mol Pharm. 2013; 10 (1): 3–10.
CAS PubMed Статья PubMed Central Google ученый
Цзэн Ц., Вэнь Х, Вэнь Ц., Чен Х, Ван И, Сюань В. и др. Вирус мозаики огурца как средство доставки доксорубицина. Биоматериалы. 2013. 34 (19): 4632–42.
CAS PubMed Статья PubMed Central Google ученый
Чой К., Ким К., Квон И.С., Ким Ай-С, Ан Х.Дж. Системная доставка миРНК с помощью химерного капсидного белка: нацеливание на опухоль и активность РНКи in vivo. Mol Pharm. 2013; 10 (1): 18–25.
CAS PubMed Статья PubMed Central Google ученый
Abbing A, Blaschke UK, Grein S, Kretschmar M, Stark CM, Thies MJ, et al. Эффективная внутриклеточная доставка белка и низкомолекулярного вещества через рекомбинантные полиомавирусоподобные частицы. J Biol Chem. 2004. 279 (26): 27410–21.
CAS PubMed Статья PubMed Central Google ученый
Якоби И., Шамис М., Бар Х, Шабат Д., Бенхар И. Нацеливание на антибактериальные агенты с помощью нитчатых бактериофагов, переносящих лекарственные средства.Антимикробные агенты Chemother. 2006. 50 (6): 2087–97.
CAS PubMed PubMed Central Статья Google ученый
Крук С.Н., Шимер Дж., Раджи И., Ву Б., Ойелере А.К., Финн М. Доставка вирусоподобных частиц в ткань легких, опосредованная макролидными антибиотиками. Mol Pharm. 2019; 16 (7): 2947–55.
CAS PubMed Статья PubMed Central Google ученый
Fasehee H, Westers H, Bolhuis A, Antelmann H, Hecker M, Quax WJ и др. Функциональный анализ сортазы YhcS в Bacillus subtilis . Протеомика. 2011. 11 (19): 3905–13.
CAS PubMed Статья PubMed Central Google ученый
Фасехи Х., Ростами А., Рамезани Ф., Ахмадиан Г. Инжиниринг E. coli клеточной поверхности с целью разработки одностадийного метода очистки рекомбинантных белков.AMB Express. 2018; 8 (1): 1–10.
CAS Статья Google ученый
Кафари С.М., Ахмадиан Г., Мохаммади М. Одностадийная очистка и ориентированное прикрепление протеина А к наночастицам диоксида кремния и оксида графена с использованием иммобилизации, опосредованной сортазой. RSC Adv. 2017; 7 (88): 56006–15.
CAS Статья Google ученый
Jegerlehner A, Tissot A, Lechner F, Sebbel P, Erdmann I, Kündig T, et al.Система молекулярной сборки, которая делает выбранные антигены очень повторяющимися для индукции защитных В-клеточных ответов. Вакцина. 2002. 20 (25–26): 3104–12.
CAS PubMed Статья PubMed Central Google ученый
Вирусоподобная частица — обзор
1.47.4.2.1 Бактерии и дрожжевые клетки
VLP структурно простых вирусов обычно образуются в бактериях или дрожжах. Три лицензированных VLP в настоящее время производятся в Saccharomyces cerevisiae : два HBV-VLP (Recombivax HB ® , Merck & Co.и Engerix-B ® , GlaxoSmithKline) и один HPV-VLP (Gardasil ® , Merck & Co.). Другой вид дрожжей, Hansenula polymorpha , был использован для производства лицензированных ВПЧ HBV (Hepavax-Gene ® , Berna Biotech Korea Corp). Другие VLP, продуцируемые дрожжами, либо в S. cerevisiae , либо в Pichia pastoris , а именно ВИЧ-VLP [32], полиомавирус-VLP [12, 129], норовирус (No) -VLP [50] и HCV -VLP [130], находятся под следствием.VLP, продуцируемые бактериями (т.е. Escherichia coli ), еще не поступили на рынок. Фактически, имеется мало или совсем нет иммуногенной информации для HBV-VLP [21], HPV-VLP [35, 37], HCV-VLP [22], Ebola-VLP [131], SV40-VLP [67], RSV- VLP [61], вирус инфекционного гиподермального и гемопоэтического некроза-VLP [132], No-VLP [133] и вирус индийского арахиса-VLP [46]. Это происходит из-за неспособности белков, экспрессируемых в прокариотических клетках, подвергаться PTM, такой как гикозилирование белков, что является ключевой особенностью большинства вакцин на основе VLP.Другой распространенной трудностью этих клеток является экспрессия растворимого и полноразмерного продукта, свободного от токсинов, белков теплового шока (HSP) и белков-шаперонов. Поскольку ограниченная растворимость рекомбинантных вирусных белков способствует образованию телец включения [35, 37], последующий процессинг значительно затруднен. Следовательно, технологический путь становится потенциально более дорогим, чем эукариотический. Даже при последующей обработке растворимых фракций предшественники VLP часто требуют разделения HSP и молекулярных белков-шаперонов (например,g., GroEL), которые могут оставаться прикрепленными к капсомерам, создавая значительную проблему биоразделения [67]. Деградация протеазы и смещение кодонов также могут быть источником снижения точности производства, способствуя более низким выходам и, возможно, неоднородности окончательной архитектуры VLP [134].
Чтобы преодолеть эти ограничения, вместо бактерий или дрожжей следует использовать системы экспрессии, такие как система бакуловирус / клетки насекомых. Другой альтернативой является разборка и повторная сборка VLP in vitro [128], метод, подробно описанный в следующих разделах.
Вирусоподобных частиц (VLP) в качестве поливалентной вакцины-кандидата против вируса чикунгунья, японского энцефалита, желтой лихорадки и вируса Зика
Синтетические генные конструкции, экспрессирующие структурные белки YFV, CHIKV и JEV, и генерация капсидного белка, содержащего VLP
Для разработки поливалентного На основе арбовирусной вакцины мы впервые разработали векторы экспрессии структурных белков для вышеуказанных вирусов. Для ZIKV, YFV и JEV он включал гены CprME, а для CHIKV — гены C-E3-E2-E1.Ранее мы разработали платформу на основе VLP для вируса Зика с использованием синтетической генной конструкции с оптимизированными кодонами 13 и использовали аналогичный подход для разработки структурных белковых конструкций для других арбовирусов с небольшими модификациями. Мы разработали консенсусную последовательность для CHIKV, JEV и YFV, чтобы включить наиболее репрезентативные последовательности циркулирующего вируса в нашу платформу вакцины. Полноразмерные геномные последовательности из базы данных ViPR использовали для создания согласованной последовательности с помощью программного обеспечения DNAStar.Затем эту консенсусную последовательность использовали для создания вектора экспрессии с оптимизированными кодонами, охватывающего структурные белки CHIKV, JEV и YFV. Последовательности с оптимизированными кодонами были синтезированы коммерчески и клонированы в вектор pcDNA 3.1 и протестированы на экспрессию белка. Как показано на фиг. 1, конструкции CHIKV, JEV и YFV показали экспрессию E после трансфекции с последующей флуоресцентной микроскопией. Для JEV и YFV экспрессия как белка E, так и белка капсида была задокументирована ( рис. 1A, C ) , а для CHIKV также могла быть обнаружена устойчивая экспрессия белка E ( рис.1E ) . Экспрессия белка ZIKV с использованием аналогичного подхода была охарактеризована ранее 13,14 .
Рисунок 1Характеристика экспрессии белков JEV, YFV и CHKV и высвобождения VLP. (A) 293 Т-клетки трансфицировали вектором экспрессии JEV CprME. Клетки анализировали на экспрессию белка E и белка капсида после окрашивания соответствующими антителами с последующей флуоресцентной микроскопией. (B) 293 Т-клетки трансфицировали одним экспрессирующим вектором JEV CprME или вектором JEV CprME вместе с экспрессионной плазмидой Zika NS2B-3.Супернатанты культур ультрацентрифугировали и анализировали на экспрессию белка E и белка капсида вестерн-блоттингом. (C) 293 Т-клетки трансфецировали вектором экспрессии CprME YFV и анализировали на экспрессию белка E и белка капсида с помощью иммунофлуоресцентной микроскопии. (D) 293 Т-клетки трансфицировали одним экспрессирующим вектором YFV CprME или вектором YFV CprME вместе с экспрессионной плазмидой Zika NS2B-3. Супернатанты культур ультрацентрифугировали и анализировали на экспрессию белка E и белка капсида вестерн-блоттингом. (E) 293 Т-клетки трансфицировали вектором экспрессии CHKV и анализировали на экспрессию белка E1-E2 с помощью иммунофлуоресцентной микроскопии. (F) Т-клетки 293 трансфицировали вектором экспрессии CHKV. Супернатанты культур ультрацентрифугировали и анализировали на экспрессию белка E1-E2 с помощью вестерн-блоттинга. Изображения A, C и E были проанализированы с использованием программного обеспечения NIS Elements AR версии 3.2 (Nikon; https://nis-elements-viewer.software.informer.com/3.2/). Изображения B, D и F были проанализированы с использованием программного обеспечения для гель-анализа GENETOOLS версии 4.03 (f) (Syngene, https://www.syngene.com/software/genetools-automatic-image-analysis/).
После успешного создания векторов экспрессии структурных белков мы затем проанализировали образование VLP из наших векторов экспрессии структурных белков с оптимизированными кодонами. Отщепление капсида от областей prME у флавивирусов опосредуется белковым комплексом NS2B-NS3, который образует активную протеазу 17 . Вирусная протеаза отщепляет белок капсида с цитоплазматической стороны ER.Это необходимо для клеточной сигналазы, чтобы отщепить и высвободить prM 17,18,19 . Экспрессия NS2B3 в транс является одним из методов предоставления протеазы для расщепления и ранее использовалась для продукции VLP вируса Зика. Мы хотели проверить, будут ли JEV и YFV CprME расщепляться протеазой Zika NS2B3. Клетки котрансфицировали ZIKV NS2B3 либо с YFV, либо с JEV CprME, и супернатанты анализировали на продукцию VLP. Как показано на фиг. 1B, конструкции D, JEV и YFV показали минимальное высвобождение VLP в супернатанты в отсутствие экспрессии NS2B3.Экспрессия протеазы значительно увеличивала секрецию VLP, что определялось как антителами E, так и CA. Более того, как ZIKV, так и WNV NS2B3 были эффективны в расщеплении ZIKV, YFV и JEV CprME со сравнимым высвобождением VLP в супернатантах ( Дополнительная фигура 1 ) . Для CHKV надежная секреция VLP была обнаружена с помощью вестерн-блоттинга при зондировании с помощью антитела E1-E2 ( фиг. 1F ) . Таким образом, наши конструкции для экспрессии CprME демонстрируют клеточную экспрессию желаемых белков, а экспрессия Zika NS2B3 с другими флавивирусными CprME может продуцировать капсидный белок, содержащий VLP.
Анализ нейтрализации на основе частиц репортерного вируса чувствителен и специфичен
Частицы репортерного вируса представляют собой специфический и чувствительный анализ для изучения различных аспектов биологии вируса, особенно проникновения вируса 20,21 . Эти псевдовирионы способны однократно инфицировать клетки способом, идентичным нативному вирусу, но не реплицируются. В случае флавивирусов структурные белки (CprME) из отдельной плазмиды могут дополнять субгеномный репликон WNV, экспрессирующий репортерный ген GFP, для генерации RVP.Было показано, что эта система на основе RVP хорошо работает с различными флавивирусами, включая WNV и Zika 13,21 . Мы создали RVP, экспрессирующие структурные белки JEV, YFV и ZIKV, и протестировали их на инфекционность в клетках Vero. Как показано на дополнительном рисунке 2A – C, клетки Vero демонстрировали инфицирование RVP JEV, YFV и ZIKV в зависимости от дозы.
Для CHIKV мы использовали несколько иной подход, поскольку это альфа-вирус. Ранее Акахата и др. . 22 , продемонстрировали, что репортерные частицы ВИЧ, псевдотипированные с помощью CHIKV Env, генерируют специфическую и чувствительную систему RVP, которую можно использовать для обнаружения нейтрализующих антител.Для разработки RVP CHIKV вектор pcDNA3.1, экспрессирующий область Env, котрансфицировали с вектором NL.LucR-E ВИЧ для получения люциферазы, экспрессирующей псевдотипированные RVP CHIKV. И снова инфицирование клеток Vero в присутствии серийных разведений CHIKV RVP показало дозозависимый сигнал люциферазы ( Дополнительный Фиг. 2D ) .
Разработав тесты на инфекционность на основе RVP для вирусов Зика, JEV, YFV и CHKV, мы затем спросили, является ли инфекция через RVP специфичной для Env и может ли она подавляться с помощью специфических сывороток.Как показано на рис. 2A – D, наблюдалась хорошая нейтрализация отдельных RVP в присутствии специфических сывороток дозозависимым образом. Более того, не наблюдалось ингибирования RVP JEV, YFV, ZIKV и CHIKV в присутствии совпадающих контрольных сывороток. Эти данные демонстрируют, что анализ на основе RVP является высокочувствительным и специфичным и может быть эффективно использован для обнаружения нейтрализующего ответа антител.
Рисунок 2Нейтрализация инфекции RVP с использованием сывороток, специфичных для заболевания.Клетки Vero инфицировали (A) RVP JEV (B) RVP YFV (C) RVP ZIKV или (D) RVP CHIKV после инкубации с серийными разведениями вирусспецифических сывороток или контрольных сывороток. Инфекция была определена через 72 часа после заражения с помощью автоматизированной микроскопии. Данные представлены как процент инфицирования, нормализованный для контрольных сывороток, как среднее значение ± стандартное отклонение трех наблюдений.
Бицистронный вектор, экспрессирующий флавивирусный CprME и Zika NS2B3, продуцирует белок капсида, содержащий VLP
Присутствие белка капсида во флавивирусной вакцине может обеспечить дополнительный иммуноген и более высокие титры нейтрализующих антител, как показано в наших исследованиях вакцины Zika VLP 13,14 .Чтобы продуцировать VLP CprME, экспрессия NS2B3 может быть достигнута либо в транс, как на фиг. 1 выше, либо с бицистронным вектором. Использование лентивирусных векторов для стабильной трансдукции клеток обеспечивает столь необходимое преимущество для создания линий клеток, секретирующих VLP. Ранее мы разработали бисцистронный вектор, который коэкспрессирует ZIKV CprME и NS2B3, используя последовательность IRES между ORF 14 . Мы использовали тот же вектор для замены Zika CprME на JEV или YFV CprME и протестировали их на продукцию VLP.Как показано на фиг. 3, бицистронные векторы приводили к устойчивой продукции VLP JEV и YFV в супернатанте, которые демонстрируют включение капсидного белка. Более того, лентивирусный вектор CHKV также показал устойчивую секрецию VLP в супернатантах культур. Таким образом, бицистронный вектор, экспрессирующий флавивирусный CprME и Zika NS2B3, надежно секретирует капсидный белок, содержащий VLP, в супернатант.
Рисунок 3Создание и характеристика бицистронных лентивирусных векторов, экспрессирующих структурные белки флавивирусов. (A) JEV CprME клонировали в лентивирусный вектор, который включал последовательность IRES, за которой следовала протеаза NS2B-3 Zika. 293 Т-клетки трансфицировали только конструкцией CprME JEV или бицистронной конструкцией лентивируса JEV. Собирали культуральные супернатанты и анализировали VLP на предмет секреции белка E и капсидного белка JEV посредством вестерн-блоттинга. (B) YFV CprME клонировали в лентивирусный вектор, как указано выше, и определяли секрецию VLP в культуральных супернатантах с помощью вестерн-блоттинга на Е и капсидный белок. (C) гены CHIKV C-E3-E2-E1 клонировали в лентивирусный вектор, и секрецию VLP определяли в супернатантах культур вестерн-блоттингом на белок E1-E2. Изображения анализировали с использованием программного обеспечения для анализа гелей GENETOOLS версии 4.03 (f). (Syngene, https://www.syngene.com/software/genetools-automatic-image-analysis/).
Создание стабильных клеточных линий, продуцирующих VLP ZIKV, YFV, JEV и CHIKV
Несколько успешных вакцин VLP в настоящее время находятся в клиническом использовании, что позволяет предположить, что этот подход коммерчески жизнеспособен 23 .Создание стабильных клеточных линий, секретирующих VLP, дает дополнительное преимущество, поскольку вакцину можно легко масштабировать для коммерческого производства. Используя бицистронный лентивирусный вектор, экспрессирующий Zika NS2B3 и флавивирусные CprME, мы создали стабильные клеточные линии, которые секретируют высокие уровни JEV, YFV ( фиг. 4A, B ) и ZIKV VLP 14 . Для CHIKV конструкция лентивируса экспрессировала область CE3E2E1. Лентивирусные частицы использовали для трансдукции Т-клеток 293 и трансдуцированных клеток, отобранных путем культивирования в присутствии бластицидина.Клоны единичных клеток характеризовали индивидуально, анализируя экспрессию белка Е с помощью проточной цитометрии и секрецию VLP в супернатанты культур. Как показано на фиг. 4A, для JEV стабильный клеточный клон JD12 был лучшим по секреции VLP и показал равномерное окрашивание белка E с помощью проточной цитометрии. Аналогичным образом клон YF9 был выбран для YFV ( фиг. 4B ) и клон Ch4 для CHKV ( фиг. 4C ) для будущего анализа. Клеточная линия ZIKV E2 была описана и охарактеризована до 14 .Используя эту стратегию, мы смогли найти клоны одиночных клеток с высоким уровнем секретирования VLP для JEV, YFV, ZIKV и CHIKV. Эти клоны клеток использовали для генерации VLP для исследований иммунизации мышей.
Рисунок 4Генерация стабильных клеточных линий, секретирующих VLP JEV, YFV и CHIKV. Т-клетки 293 трансдуцировали (A) JEV, (B) YFV или (C) CHKV структурным белком, содержащим частицы лентивируса. Трансдуцированные клетки отбирали бластицидином в массе с последующим клонированием единичных клеток с ограниченным разведением.Для каждого вируса несколько клонов одиночных клеток были охарактеризованы на предмет окрашивания белка оболочки на поверхности клетки с помощью проточной цитометрии и секреции VLP в культуральные супернатанты с помощью вестерн-блоттинга. Средняя интенсивность флуоресценции (MFI) окрашивания белка оболочки для различных клонов отдельных клеток для JEV, YFV и CHIKV показана справа. Изображения гелей анализировали с использованием программного обеспечения для анализа гелей GENETOOLS версии 4.03 (f) (Syngene, https://www.syngene.com/software/genetools-automatic-image-analysis/).Гистограммы проточной цитометрии были созданы с использованием программного обеспечения FloJo версии 10.6.0 (Tree Star, https://www.flowjo.com/solutions/flowjo/downloads).
Тестирование стабильности клонов единичных клеток, продуцирующих различные VLP
Для того, чтобы вакцина-кандидат была успешной, желательно, чтобы была минимальная вариабельность между препаратами и клеточная линия была стабильной и не теряла экспрессию экзогенного гена. Крупномасштабное расширение также потребует роста клеток в среде, свободной от агентов отбора, таких как бластицидин.Чтобы удовлетворить вышеуказанным критериям, мы проверили стабильность клеточных линий двумя отдельными методами. Клетки культивировали в присутствии бластицидина в течение ~ 9 месяцев. После этого клетки окрашивали на экспрессию Е и капсидного белка и анализировали с помощью флуоресцентной микроскопии. Как показано на фиг. 5A, стабильные клеточные линии показали устойчивую экспрессию белков E и Capsid, несмотря на длительное культивирование, что свидетельствует о стабильной интеграции экзогенного гена. Затем мы спросили, способны ли клеточные линии к устойчивой секреции VLP в отсутствие бластицидина, что может быть желательно во время массового приготовления вакцины.Для этого клеточные линии культивировали в отсутствие бластицидина в течение 30 дней. После терминального пассажа и когда клетки достигли слияния, культуральные супернатанты концентрировали и анализировали на секрецию VLP посредством вестерн-блоттинга. Для сравнения использовали клетки, культивированные рядом в присутствии бластицидина. Как показано на фиг. 5B, клетки, культивируемые в отсутствие бластицидина, показали сравнимую продукцию VLP для всех четырех клеточных линий (JEV, CHIKV, YFV и ZIKV), как и клетки, культивируемые в присутствии бластицидина.Затем мы проанализировали морфологию VLP, полученных из стабильных клеточных линий после длительного культивирования. Морфология частиц JEV, CHIKV, YFV и ZIKV соответствовала морфологии вирусных частиц со средним диаметром 40-50 нм или немного больше для CHIKV и плотно окрашенных мембран, как продемонстрировано с помощью электронной микроскопии ( Рис. 5C ) . Эти данные демонстрируют, что полученные клоны единичных клеток демонстрируют стабильное включение экзогенного гена в течение длительного периода времени и демонстрируют устойчивую секрецию VLP в отсутствие бластицидина.
Рисунок 5Характеристика стабильных клонов одиночных клеток. (A) Клеточные линии JEV-JD12, YFV-YF9 и CHIKV-Ch4 окрашивали на экспрессию белка E и / или капсида. Клетки анализировали с помощью флуоресцентной микроскопии и получали изображения. (B) Стабильные клеточные линии культивировали в присутствии (+) или отсутствии (-) бластицидина в течение 30 дней с обычным субкультивированием. Супернатанты культур анализировали на экспрессию белка Е с помощью вестерн-блоттинга.M = маркер молекулярной массы белка. (C) VLP, собранные из отдельных стабильных клеточных линий, отрицательно окрашивали и анализировали с помощью просвечивающей электронной микроскопии. Масштаб = 50 нм. Изображения флуоресцентной микроскопии анализировали с помощью программного обеспечения NIS Elements AR версии 3.2 (Nikon; https://nis-elements-viewer.software.informer.com/3.2/). Изображения гелей анализировали с использованием программного обеспечения для анализа гелей GENETOOLS версии 4.03 (f) (Syngene, https://www.syngene.com/software/genetools-automatic-image-analysis/).
Иммунизация мышей моновалентной, двухвалентной или четырехвалентной (CJaYZ) арбовирусной вакциной индуцирует высокие уровни нейтрализующих антител
Разработав надежную систему для получения VLP, мы затем приступили к тестированию иммуногенности поливалентной вакцины на мышиной модели. Поскольку вакцина производится в виде индивидуальных VLP (, дополнительная фиг. 3A, ) , важно протестировать моновалентный состав вместе с двухвалентными или четырехвалентными комбинациями.Мы включили двухвалентный состав, который включал VLP JEV и CHIKV, поскольку эти два вируса распространены в Азии, и вторую бивалентную группу, состоящую из VLP YFV и CHIKV, поскольку эти два вируса являются эндемичными в Южной Америке и Африке 1 . Мышей Balb / c группами по 6 человек иммунизировали моновалентными, двухвалентными или четырехвалентными VLP в комплексе с квасцами (2% альгидрогеля) в качестве адъюванта. Содержание белка в отдельных препаратах VLP и поливалентном составе было сопоставимым (дополнительная фигура 3B ) .Две иммунизации проводили на неделе 0 и неделе 2, и образцы сыворотки собирали примерно через 6 недель после первичной иммунизации (, дополнительная фиг. 3C ) .
Сыворотки иммунизированных мышей тестировали на образование нейтрализующих антител с использованием анализа RVP. Как показано на рис. 6A – D, высокие уровни нейтрализующих антител были обнаружены во всех группах иммунизированных мышей. Как и ожидалось, титры были самыми высокими для моновалентных групп, поскольку они получали самую высокую дозу антигена.Мыши, иммунизированные комбинациями двух- и четырехвалентных вакцин, показали небольшое снижение титров нейтрализующих антител, вероятно, из-за уменьшения дозы антигена. Эти данные демонстрируют возможность мультивалентной арбовирусной вакцины вызывать сильный нейтрализующий ответ антител.
Рисунок 6Эффективность нейтрализации комбинаций вакцин с VLP. Сыворотки, полученные от мышей, иммунизированных различными комбинациями вакцин VLP, анализировали на выработку нейтрализующего ответа антител.Анализы на основе репортерного вируса использовали для определения эффективности нейтрализующих антител, строили кривые и определяли значения EC50. Показаны значения EC50 нейтрализации (A), JEV, (B), YFV, (C), ZIKV и (D), CHIKV для каждой мыши. Все образцы были проанализированы в двух экземплярах.
Характеристика иммунного ответа, генерируемого после иммунизации мышей вышеуказанными комбинациями вакцин
Наши данные на фиг. 6 ясно демонстрируют, что иммунизация мышей моновалентной, двухвалентной и четырехвалентной вакциной CJaYZ индуцирует мощный нейтрализующий ответ антител.Затем мы рассмотрели характеристики специфических антител, вырабатываемых у иммунизированных мышей. Для этого клеточные лизаты ZIKV, JEV, YFV и CHIKV. VLP, секретирующие стабильные клеточные линии, подвергали иммунопреципитации с объединенными сыворотками, полученными от различных групп иммунизированных мышей. Как показано на фиг. 7A и согласуется с данными о нейтрализующих антителах, моновалентная вакцина VLP CHIKV генерировала самые сильные титры антител, за которыми следовали двухвалентные и четырехвалентные комбинации. Интересно, что для CHIKV генерация капсидных антител была очень устойчивой и также следовала падающей схеме в двухвалентных и четырехвалентных комбинациях.Это ясно демонстрирует присутствие капсидного белка в VLP CHIKV и генерацию антикапсидного иммунного ответа при иммунизации. Для YFV, JEV и ZIKV ( Рис. 7B – D ) снова специфические антитела E и prM были детектированы максимально в моновалентной вакцине со снижением уровней в двухвалентных и четырехвалентных комбинациях. В целом, эти данные демонстрируют образование специфических антител к YFV, JEV, ZIKV и CHIKV E, prM и Capsid при иммунизации поливалентной вакциной VLP.
Фиг. 7Качество ответа антител, генерируемого у мышей, иммунизированных VLP. (A) Стабильная линия клеток CHIKV-E3-E2-E1 была радиоактивно помечена [35S] Met-Cyst, и клеточные лизаты подверглись иммунопреципитации объединенными сыворотками от указанных групп иммунизированных мышей. Комплексы разделяли на геле SDS-PAGE с последующей флюорографией. (B) Стабильная клеточная линия YFV-CprME была радиоактивно помечена [35S] Met-Cyst, и клеточные лизаты иммунопреципитированы объединенными сыворотками от соответствующих групп иммунизированных мышей. (C) Стабильная линия клеток JEV-CprME была радиоактивно помечена [35S] Met-Cyst, и клеточные лизаты иммунопреципитированы объединенными сыворотками от указанных групп иммунизированных мышей. (D) Стабильная клеточная линия ZIKV-CprME была радиоактивно помечена [35S] Met-Cyst, и клеточные лизаты иммунопреципитированы объединенными сыворотками от указанных групп иммунизированных мышей. Количественное определение полос для Env, prM и капсидного белка показано на графиках рядом с каждым гелем. Изображения гелей анализировали с использованием программного обеспечения Multi Gauge версии 3.0 (http://www.winsite.com/fujifilm/fujifilm+multigauge/).
Адаптация клеточных линий к суспензионному росту и в бессывороточной среде для быстро масштабируемого производства VLP
Коммерческий успех вакцин VLP основан на культивировании большого объема клеточных линий в биореакторах. Более того, размножение клеток в бессывороточной среде позволяет исключить нежелательные белки, присутствующие в сыворотке. Хотя линии клеток на основе 293 Т, полученные в нашем исследовании, продуцируют большое количество VLP, адаптация этих клеток к росту в суспензии будет способствовать коммерческому успеху платформы вакцины.293 Т-клетки поддаются адаптации к суспензии с использованием специализированных сред и особых условий культивирования 24 . Мы адаптировали клетки для роста в суспензии, культивируя их в колбах Эрленмейера объемом 125 мл в бессывороточной среде EX CELL. Клетки пассировали несколько раз и тестировали на присутствие антигена E с помощью проточной цитометрии и секреции VLP с помощью вестерн-блоттинга. Как показано на фиг. 8C, адаптация клеток к росту суспензии изменила морфологию клеток, сделав их округлыми и отделенными по сравнению с их прилипшими аналогами.Окрашивание для экспрессии белка E на поверхности клетки было сопоставимым между прикрепленными и суспензионными клетками ( фиг. 8A ) . Интересно, что секреция VLP для суспензионных клеток оказалась намного выше в супернатанте по сравнению с таким же объемом супернатантов адгезивных клеток ( фиг. 8B ) . Вероятно, это связано с ростом клеток до более высокой плотности в суспензионной культуре по сравнению с прикрепленными клетками. Эти данные демонстрируют возможность адаптации стабильных клеточных линий к росту суспензии в отсутствие белков сыворотки, которые секретируют высокие концентрации VLP в супернатантах культур.
Рисунок 8Адаптация стабильных клеточных линий для роста в суспензионной культуре. (A) Стабильные клеточные линии JEV, YFV, ZIKV и CHIKV были адаптированы для роста в суспензионной культуре. После полной адаптации клетки окрашивали на экспрессию белка Е с помощью проточной цитометрии. Соответствующие прилипшие аналоги использовались одновременно в качестве контроля окрашивания. (B) Продукция VLP из адаптированных суспензионных клеточных линий определялась вестерн-блоттингом для белка E и сравнивалась с секрецией VLP из соответствующих прикрепленных аналогов. (C) Морфология суспензионных клеточных линий с помощью светлопольной микроскопии и сравнение с их соответствующими адгезивными аналогами. Гистограммы проточной цитометрии были созданы с использованием программного обеспечения FloJo версии 10.6.0 (Tree Star, https://www.flowjo.com/solutions/flowjo/downloads). Изображения гелей анализировали с использованием программного обеспечения для анализа гелей GENETOOLS версии 4.03 (f) (Syngene, https://www.syngene.com/software/genetools-automatic-image-analysis/). Изображения в ярком поле анализировали с помощью программного обеспечения NIS Elements AR версии 3.2 (Nikon, https://nis-elements-viewer.software.informer.com/3.2/).
Произошла ошибка при настройке пользовательского файла cookie
Этот сайт использует файлы cookie для повышения производительности. Если ваш браузер не принимает файлы cookie, вы не можете просматривать этот сайт.
Настройка вашего браузера для приема файлов cookie
Существует множество причин, по которым cookie не может быть установлен правильно. Ниже приведены наиболее частые причины:
- В вашем браузере отключены файлы cookie.Вам необходимо сбросить настройки вашего браузера, чтобы он принимал файлы cookie, или чтобы спросить вас, хотите ли вы принимать файлы cookie.
- Ваш браузер спрашивает вас, хотите ли вы принимать файлы cookie, и вы отказались. Чтобы принять файлы cookie с этого сайта, используйте кнопку «Назад» и примите файлы cookie.
- Ваш браузер не поддерживает файлы cookie. Если вы подозреваете это, попробуйте другой браузер.
- Дата на вашем компьютере в прошлом. Если часы вашего компьютера показывают дату до 1 января 1970 г., браузер автоматически забудет файл cookie.Чтобы исправить это, установите правильное время и дату на своем компьютере.
- Вы установили приложение, которое отслеживает или блокирует установку файлов cookie. Вы должны отключить приложение при входе в систему или проконсультироваться с системным администратором.
Почему этому сайту требуются файлы cookie?
Этот сайт использует файлы cookie для повышения производительности, запоминая, что вы вошли в систему, когда переходите со страницы на страницу. Чтобы предоставить доступ без файлов cookie потребует, чтобы сайт создавал новый сеанс для каждой посещаемой страницы, что замедляет работу системы до неприемлемого уровня.
Что сохраняется в файле cookie?
Этот сайт не хранит ничего, кроме автоматически сгенерированного идентификатора сеанса в cookie; никакая другая информация не фиксируется.
Как правило, в файлах cookie может храниться только информация, которую вы предоставляете, или выбор, который вы делаете при посещении веб-сайта. Например, сайт не может определить ваше имя электронной почты, пока вы не введете его. Разрешение веб-сайту создавать файлы cookie не дает этому или любому другому сайту доступа к остальной части вашего компьютера, и только сайт, который создал файл cookie, может его прочитать.
Быстрое образование частиц, подобных вирусу иммунодефицита человека
Наши текущие знания кинетики сборки отдельных ретровирусов основаны исключительно на исследованиях динамики флуоресцентных точек, наблюдаемых с помощью флуоресцентной микроскопии полного внутреннего отражения (TIRFM) базальной мембраны адгезивных клеток, экспрессирующих вирусный полипротеин Gag, слитый с флуоресцентными белками, например зеленым флуоресцентным белком (GFP) (1⇓ – 3). Gag является основным структурным белком ретровирусов, и его экспрессии достаточно, чтобы управлять образованием вирусоподобных частиц (VLP) (4).В TIRFM глубина резкости составляет ~ 200 нм над границей раздела стекло / поверхность. Это сводит к минимуму расфокусированную, «фоновую» флуоресценцию внутри клеток и обеспечивает изображения с достаточным контрастом для четкого обнаружения ограниченных дифракцией флуоресцентных пятен, представляющих предполагаемые отдельные VLP на базальной поверхности клетки. Остается неясным, мешает ли узкое расстояние между клеточной мембраной и стеклом формированию и высвобождению вирусных частиц диаметром 120 нм. Предположение о том, что динамика GFP-меченных пятен Gag может служить моделью для образования вирусных частиц с немодифицированным Gag, основано на том факте, что многие из этих пятен колокализуются с почковыми структурами с помощью корреляционных изображений с помощью световой и электронной микроскопии (CLEM) ( 5).Однако это последнее исследование также сообщает, что многие из наблюдаемых пятен GFP не соответствуют ассоциированным с мембраной зачаткам или VLP, видимым с помощью ЭМ. Таким образом, степень, в которой GFP (прикрепленный к Gag) влияет на сборку и морфологию VLP, остается неясной, поскольку опубликованные результаты различаются (5, 6). Чтобы попытаться избежать потенциальных артефактов GFP-тегирования, немеченый Gag обычно котрансфицируется с Gag-GFP в соотношениях от 1: 1 до 1:10. Следовательно, широкий диапазон стехиометрии меченого и немеченого Gag вероятен на уровне отдельной клетки, что приводит к гетерогенному содержанию Gag-GFP и немеченому Gag внутри VLP (7).
Здесь мы использовали высокоскоростную (HS), коррелятивную сканирующую микроскопию ионной проводимости и флуоресцентную конфокальную микроскопию (SICM-FCM) визуализацию живых клеток, чтобы охарактеризовать и сравнить образование VLP ВИЧ на верхних поверхностях клеток, в отличие от нижняя поверхность, контактирующая со стеклянным покровным стеклом, обычно изучается методом TIRFM. Наблюдения проводились на клетках Jurkat, HeLa, Cos-7 и HEK293T, экспрессирующих меченый и немеченый Gag ВИЧ. SICM — это метод бесконтактной сканирующей зондовой микроскопии, который может отображать и измерять трехмерную морфологию клеток в физиологических буферах с высоким пространственным разрешением (8, 9).Корреляционный SICM-FCM, аналогичный CLEM, создает пары изображений поверхности и флуоресценции, которые могут быть наложены друг на друга для установления корреляции. Однако, в отличие от CLEM, SICM-FCM — это метод визуализации в реальном времени, который может отслеживать морфологические изменения процессов, происходящих на поверхности клетки, такие как эндоцитоз и поглощение вирусов и наночастиц (10–12). Здесь мы показываем, что сборка и высвобождение VLP с верхней, беспрепятственной поверхности клеток может быть в 20 раз быстрее, чем сообщалось для VLP отростка из плазматической мембраны (PM) в контакте со стеклянной подложкой с помощью TIRFM.Кроме того, топологические изменения, связанные с почкованием VLP, значительно варьируются в зависимости от используемой клеточной модели и вирусного белка, который помечен.
Результаты
Образование VLP в клетках Jurkat.
Мы визуализировали клетки Jurkat-TAg, трансфицированные ph3B-mPlum / Gag (7), с использованием недавно разработанной системы HS-SICM. Клетки, экспрессирующие немеченый Gag, идентифицировали по экспрессии флуоресцентно меченного гистона. Топографические изображения SICM трансфицированных клеток, зафиксированные через 14 часов после трансфекции, выявили выступы PM, которые по размеру и форме можно было идентифицировать как почкующиеся VLP (рис.1 A и B ). Изображения просвечивающей электронной микроскопии (ПЭМ) подтвердили образование VLP с ВИЧ-подобным внешним видом и размерами, аналогичными тем, которые наблюдались с помощью SICM (рис. 1 C и D ). SICM- и TEM-изображения нетрансфицированных клеток Jurkat показали, что эти клетки имеют гладкую поверхность, украшенную редкими микроворсинками (∼400 нм в диаметре и длиной до нескольких микрометров), и не имеют выступов PM, которые топографически можно спутать с VLP или зачатками VLP ( SI Приложение , рис.S1 A ). Клетки Jurkat, экспрессирующие h3B-mPlum / Gag, образовывали VLP с высокой эффективностью, причем VLP обнаруживали на 24 из 30 визуализированных клеток, зафиксированных между 14 и 24 часами после трансфекции. SICM-изображения клеток, зафиксированных через 24 часа, показали, что количество VLP на PM увеличивалось со временем ( SI, приложение , рис. S1 B ). Путем иммуноокрашивания мы подтвердили отсутствие тезерина и TIM-1 (Т-клеточный иммуноглобулин и домен муцина 1), которые могли бы закрепить высвободившиеся VLP на PM ( SI, приложение , рис.S1 C и D ) (13, 14). Также ранее было продемонстрировано, что клетки Jurkat не экспрессируют белки тезерин и TIM-1 (15, 16). Обработка живых клеток протеазой 100 мкг / мл Bacillus licheniformis Субтилизин A привела к быстрому снижению на 72 ± 21% (два независимых эксперимента) количества поверхностно-связанных VLP ( SI Приложение , рис. S1 E и F ), что указывает на то, что большинство наблюдаемых VLP-подобных структур завершили расщепление, но остались прикрепленными к PM либо с помощью тезерина, либо с помощью TIM-1, присутствующего на поверхности клеток на неопределяемых уровнях, или, возможно, с помощью альтернативы, пока -неопределенные, белковые ссылки.
Рис. 1. ОбразованиеVLP ВИЧ на клетках Jurkat, трансфицированных h3B-mPlum / Gag. ( A ) SICM-изображение VLP на клетке, зафиксированной через 14 часов после трансфекции. ( B ) Профиль поперечного сечения выступа мембраны (черная линия), соответствующий типичному предполагаемому Gag VLP из A ; пунктирная окружность представляет собой VLP диаметром 125 нм, помещенную в профиль для справки. ( C и D ) ПЭМ-изображения клеток, зафиксированных через 19 ч после трансфекции, показывающие VLP.( E ) Покадровые изображения HS-SICM, показывающие образование и исчезновение VLP (красные стрелки), записанные, начиная с 8 часов после трансфекции. Изображения получены со скоростью 8,6 кадра в минуту. ( F ) Высота и диаметр (ширина) зачатка VLP, измеренные на топографических изображениях SICM. ( G ) Среднее изменение высоты VLP во время сборки ( n = 32, выровнено по зарождению, слева ) и до выпуска ( n = 42, выровнено по исчезновению, справа ).( H ) Распределение времен жизни VLP. (Масштабные линейки ТЕМ: 1 мкм в C и 200 нм в D .)
Затем мы проследили отдельные события формирования и высвобождения VLP, управляемые Gag, в живых клетках со скоростью сканирования от 8,6 до 4,3 кадра в минуту (от 7 до 14 с на кадр) (рис.1 E ). Сравнение выступов PM на топографических изображениях фиксированных и живых клеток SICM показало схожие высоты (медиана = 117 нм, межквартильный диапазон [IQR] = 140–90, n = 100, фиксированный и 122 нм, IQR = 140–110, n = 181, живой) и диаметры (127 нм, IQR = от 147 до 110, n = 100, фиксированный и 118 нм, IQR = 130 до 110, n = 181, live) (рис.1 F ). Сборка VLP характеризовалась постепенным увеличением измеренной высоты выступов, которая в среднем достигала максимума через 21 с (рис. 1 G , Left ). Резкое исчезновение всей структуры было интерпретировано как высвобождение VLP из клеточной мембраны (рис. 1 G , справа ). Всего мы проследили 267 индивидуальных VLP (48 клеток, 10 экспериментов) от момента начального искривления мембраны до полного исчезновения топографически обнаруженных выступов.Анализ времени жизни VLP показал бимодальное распределение с пиками при 28 и 194 с (рис. 1 H ). Третью группу выступов, возможно, с еще более длительным сроком службы, невозможно было отследить, когда они попадали в зону наблюдения и выходили из нее; они, вероятно, представляют собой VLP, которые не смогли завершить расслоение или остались связанными с мембраной после завершения сборки. Отслеживание образования VLP в живых клетках в присутствии 100 мкг / мл субтилизина А привело к средней продолжительности жизни 42 с (медиана, IQR = от 48 до 24, n = 20, шесть клеток, один эксперимент).Это больше, чем среднее время жизни короткоживущих VLP на необработанных клетках, возможно, из-за пагубного воздействия протеазы на живые клетки, которое часто приводило к отслоению клеток от субстрата.
Чтобы подтвердить, что наблюдаемые выступы мембраны представляют собой VLP, образованные Gag, и сравнить динамику VLP, образованных меченым и немеченым Gag, мы визуализировали клетки Jurkat, трансфицированные 1: 1 Gag-GFP: SynGP с помощью коррелятивного SICM-FCM. . SynGP — это синтетический Gag-Pol с оптимизированными кодонами, который может формировать протеолитически зрелые VLP ВИЧ (17).Изображения SICM-FCM выявили многочисленные выступы мембраны (рис. 2 A , слева ) и отчетливые пятна флуоресценции Gag-GFP (рис. 2 A , средний ). Анализ наложенных флуоресцентных и топографических изображений (рис. 2 A , справа ) Gag-GFP-положительных клеток, зафиксированных через 18 и 24 ч после трансфекции (16 и 14 клеток, соответственно), показал, что только пять клеток продуцировали Gag-GFP. пятна флуоресценции, которые коррелировали с топографически обнаруженными зачатками VLP (рис.2 А ). Большинство, 17 клеток, продуцировали пятна флуоресценции Gag-GFP, которые коррелировали с плоскими или слегка изогнутыми участками мембраны (рис. 2 B ). В этих 22 клетках мы идентифицировали в общей сложности 462 пятна флуоресценции Gag-GFP и 192 топографически обнаруженных зачатка VLP, из которых 119 перекрывались (т. Е. 26% пятен флуоресценции Gag-GFP коррелировали со структурами почкования, а 62% топографически обнаруженных зачатков имели ассоциированная флуоресценция). В совокупности эти данные представлены в виде диаграммы Эйлера на рис.2 С . Мы не наблюдали увеличения количества пятен Gag-GFP, связанных с топографически определяемыми почками между 18 и 24 часами после трансфекции. Остальные восемь клеток продуцировали в основном однородные внутриклеточные или нечеткие пятна флуоресценции, которые не соответствовали VLP-подобным топографическим структурам. Средняя высота и диаметр Gag-GFP-положительных зачатков составляли 110 нм (IQR = 140–100, n = 39) и 140 нм (IQR = 160–125, n = 39), соответственно, аналогично размерам VLP. формируется на клетках Jurkat, трансфицированных ph3B-mPlum / Gag ( SI Приложение , рис.S1 G ). В соответствии с наблюдениями SICM-FCM, ПЭМ-изображения клеток, положительных по флуоресценции Gag-GFP, показали присутствие преимущественно плоских или изогнутых сборок Gag (рис.2 D ), хотя подробное изучение изображений TEM выявило неоднородности в слое Gag VLP. аналогичны ранее опубликованным структурам (18) и предположительно вызваны присутствием GFP (рис. 2D, справа, , стрелка).
Рис. 2. ОбразованиеVLP ВИЧ в клетках Jurkat, трансфицированных 1: 1 Gag-GFP и SynGP.( A и B ) Корреляционные изображения фиксированных клеток SICM-FCM, демонстрирующие примеры корреляции между флуоресценцией Gag-GFP и зачатками VLP: топографическое изображение SICM ( слева, ), конфокальное флуоресцентное изображение (, среднее ) и наложение ( Правый ). ( C ) Диаграмма Эйлера, показывающая взаимосвязь в наборах пятен флуоресценции Gag-GFP и топографически обнаруженных почек. ( D ) ПЭМ-изображения почек VLP; черная стрелка указывает на разрыв в слое Gag.(Масштаб: 200 нм.) ( E ) Цейтраферные изображения SICM-FCM, показывающие образование и исчезновение VLP (красные стрелки). Изображения получены с частотой один кадр в минуту. ( F ) Распределение продолжительности жизни Gag-GFP-положительных почек. ( Вставка ) Высота бутона (черная линия) и следы интенсивности флуоресценции (зеленая линия) для VLP в E .
Учитывая низкую вероятность обнаружения почек, связанных с флуоресценцией Gag-GFP, мы увеличили размер сканирования покадровых изображений SICM-FCM до 4 × 4 мкм.Это снизило частоту кадров до одного кадра в минуту. В 83 клетках из 22 независимых экспериментов мы зарегистрировали в общей сложности 25 событий, в которых наблюдалась четкая корреляция между флуоресценцией Gag-GFP и топографически обнаруженными почковыми структурами от зарождения зачатка до его исчезновения вместе с связанной с ним флуоресценцией Gag-GFP (рис. 2 E ). Появление флуоресценции Gag-GFP на детектируемом уровне предшествовало формированию зачатков, что указывает на прогрессивную сборку Gag в VLP (рис.2 F , Врезка ). Мы зарегистрировали среднее время жизни почкования 134 ± 30 с (рис. 2 F ). Хотя это было ограничено частотой кадров, это похоже на более медленную популяцию VLP, наблюдаемую в клетках, трансфицированных h3B-mPlum / Gag.
Чтобы попытаться уменьшить любое потенциальное вмешательство флуоресцентной метки в образование VLP и улучшить корреляцию между топографически обнаруживаемыми зачатками VLP и флуоресцентным сигналом, мы проверили, можно ли использовать вирусный белок R (Vpr), меченный GFP (Vpr-GFP), в качестве альтернативный маркер сборки вириона.Vpr не является структурным белком ВИЧ, но он включается в вирионы на относительно низких уровнях (по сравнению с Gag) и используется для переноса флуоресцентных белков для мечения инфекционных вирусных частиц (19). Согласно литературным данным, количество молекул Vpr на один вирион в трансфицированных клетках может составлять от 250 до 500 в зависимости от уровня экспрессии Vpr (20, 21). Хотя уровни флуоресценции Vpr-GFP были заметно ниже, чем у Gag-GFP, что делало корреляцию менее надежной, 1: 1 Vpr-GFP: SynGP приводил к эффективному образованию топографически определяемых зачатков, которые коррелировали с пятнами флуоресценции Vpr-GFP.Мы обнаружили корреляцию в 5 из 13 клеток, зафиксированных через 18 часов, и в 7 из 9 клеток, зафиксированных через 24 часа после трансфекции (рис. 3 A ). В этих 12 клетках мы идентифицировали всего 488 пятен флуоресценции Vpr-GFP и 489 топографически обнаруженных зачатков VLP, из которых 475 перекрывались. Следовательно, более 97% пятен флуоресценции Vpr-GFP коррелировали со структурами почкования, и более 80% топографически обнаруженных почек имели ассоциированную флуоресценцию (Рис. 3 B ). Средняя высота и диаметр бутонов составляли 110 нм (IQR = 130–90, n = 57) и 120 нм (IQR = 170–120, n = 57), соответственно, аналогично размерам образовавшихся VLP. в клетках Jurkat, трансфицированных ph3B-mPlum / Gag ( SI Приложение , рис.S1 G ).
Рис. 3. ОбразованиеVLP ВИЧ в клетках Jurkat, трансфицированных 1: 1 Vpr-GFP и SynGP. ( A ) SICM-FCM изображения фиксированной клетки, показывающие корреляцию между флуоресценцией Vpr-GFP и зачатками VLP. ( B ) Диаграмма Эйлера, показывающая относительное перекрытие пятен флуоресценции Vpr-GFP и топографически обнаруженных зачатков. ( C ) Покадровые изображения SICM-FCM, показывающие образование и исчезновение VLP (красные стрелки). Изображения были получены со скоростью 4,3 кадра в минуту.( D ) Распределение продолжительности жизни положительных почек Vpr-GFP. ( Вставка ) Следы высоты бутона (черная линия) и интенсивности флуоресценции (зеленая линия) для VLP в C .
В 75 клетках из 18 независимых экспериментов мы идентифицировали и проследили 34 почкующиеся структуры, которые коррелировали с флуоресценцией Vpr-GFP от момента зарождения до исчезновения с частотой кадров, варьирующейся от 4,3 до 2 кадров в минуту (Рис. 3 C ). Распределение времени наблюдения VLP лучше всего соответствовало экспоненциальному затуханию и имело период полураспада 40 с (рис.3 D ). Это распределение, вероятно, будет ограничено скоростью сканирования и низкой вероятностью обнаружения успешных событий бутонизации из-за того, что VLP дрейфуют в зоне наблюдения и из нее. Для сравнения, VLP, образованные немеченым Gag, показанные на фиг. 1 H , имели период полураспада 51 с при экспоненциальной аппроксимации. Подобно Gag-GFP, появление флуоресценции Vpr-GFP на детектируемом уровне предшествовало формированию топографически детектируемых зачатков, что указывает на раннее рекрутирование Vpr в VLP (рис.3 D , врезка ).
Вместе эти данные показывают, что почкование немеченых и флуоресцентно меченых вирусов может отслеживаться в живых клетках на уровне отдельных частиц с помощью SICM-FCM. Важно отметить, что кинетика топологических изменений, связанных с образованием зачатков, управляемым Gag, указывает на то, что сборка и высвобождение VLP ВИЧ может быть быстрее, чем сообщалось ранее с использованием TIRFM (1–3). Мы также демонстрируем, что флуоресцентное мечение Gag, например, путем вставки GFP, может изменять организацию Gag в PM и влиять на кинетику образования VLP.
Формирование VLP в клетках HeLa.
Чтобы сравнить наши результаты с ранее опубликованными наблюдениями, мы проанализировали образование VLP с помощью SICM-FCM и TEM в клетках HeLa, так как большинство исследований TIRFM кинетики сборки ВИЧ-1 проводилось на этом типе клеток (1–3). Однако топографические изображения SICM верхней поверхности нетрансфицированных фиксированных клеток HeLa выявили многочисленные мембранные выступы, соответствующие микроворсинкам и дорсальным складкам, некоторые из которых можно было спутать с полностью сформированными зачатками и VLP (рис.4 А ). Мы в целом классифицировали эти выступы на три категории: 1) круглые, похожие на культю выступы (красная стрелка) со средней высотой 272,5 нм (медиана, IQR = 220-425, n = 42) и диаметром 160 нм (IQR = 150–165, n = 42), соответствующие микроворсинкам, 2) пальцеобразные выступы (черная стрелка), соответствующие спинным филоподиям или микроворсинкам, и 3) мембранные лоскуты, соответствующие оборкам (голубая стрелка). Доля культи, пальцевидных микроворсинок и дорсальных складок значительно варьировала от клетки к клетке ( SI Приложение , рис.S2 A и C ).
Рис. 4. ОбразованиеVLP ВИЧ на клетках HeLa. ( A ) Топографическое изображение SICM нетрансфицированной клетки HeLa (фиксированное), показывающее выступы мембраны, соответствующие коротким, похожим на культю микроворсинкам (красная стрелка), длинным пальцевидным микроворсинкам (черная стрелка) и спинным складкам (голубая стрелка) . ( B ) Корреляционные изображения SICM-FCM верхней поверхности фиксированной клетки HeLa, трансфицированной Gag-GFP. Красные стрелки указывают на мембранные зачатки, с которыми связана флуоресценция Gag-GFP.( C ) Пеньковидный выступ и высота и диаметр (ширина) зачатка мембраны, измеренные на топографических изображениях SICM нетрансфицированных ( n = 42, шесть клеток) и трансфицированных Gag-GFP клеток, индивидуально для зачатков с ( n = 40) и без ( n = 47) соответствующих пятен флуоресценции Gag-GFP (пять клеток) (двухвыборочный тест t , * P <0,05, ** P <0,01). ( D ) Диаграмма Эйлера, показывающая относительное перекрытие флуоресцентных пятен Gag-GFP и топографически обнаруженных зачатков.( E ) Профиль поперечного сечения выступа мембраны, соответствующий типичному Gag VLP, измеренному в B ( справа , красная линия). ( F ) Профиль поперечного сечения выступа мембраны, соответствующий типичной микроворсинки в D , черная линия. ( G ) ТЕМ-изображение иммуномеченого криосреза клеток HeLa, трансфицированных Gag-GFP. Красная стрелка указывает кляп на кончике микроворсинки. ( H ) ТЕМ-изображения VLP и зачатков Gag, сформированных на неограниченной мембране ( верх ) и ограниченной мембране в межклеточном контакте ( низ ) одной и той же клетки HeLa, трансфицированной Gag-SNAP.Белые стрелки указывают на разрывы в слое Gag. Кроличьи анти-p24 / протеин A-gold используются в изображениях ПЭМ. (Масштаб: 200 нм.)
Корреляционная визуализация SICM-FCM клеток HeLa, временно трансфицированных Gag-GFP, также выявила многочисленные выступы мембраны (рис. 4 B , слева ) и отчетливые пятна флуоресценции Gag-GFP в конфокальные изображения поверхности (рис. 4 B , Middle ). Наложение флуоресценции и топографические изображения показали, что многие выступы, похожие на пень, имеют ассоциированную флуоресценцию Gag-GFP (рис.4 B , справа , красные стрелки). Однако мы также наблюдали флуоресценцию Gag-GFP, связанную с пальцеобразными микроворсинками и спинными складками, а также с плоскими участками мембран ( SI Приложение , рис. S2 B и D ). Чтобы выяснить, могут ли флуоресцентные культеподобные выступы быть VLPs, мы сравнили их высоту и диаметр с аналогичными нефлуоресцентными выступами в Gag-GFP-экспрессирующих клетках и выступами в нетрансфицированных клетках (Fig. 4 C ).Мы обнаружили, что, хотя высота выступов Gag-GFP-положительной мембраны составляла 210 нм (IQR = 145-300, n = 40), то есть почти в два раза больше диаметра средней VLP, она также была значительно ниже по сравнению с высота Gag-GFP – отрицательных выступов (350 нм, IQR = 200–450, n = 47). Большой разброс измеренных высот предполагал, что эти структуры были микроворсинками, которые в момент фиксации подвергались активному росту или ретракции (22). Диаметры Gag-GFP-положительных и отрицательных выступов существенно не различались (160 нм [IQR = от 125 до 185, n = 40] и 175 нм [IQR = 155 до 190, n = 47], соответственно. ).Мы идентифицировали в общей сложности 312 пятен флуоресценции Gag-GFP и 343 топографически обнаруженных зачатка VLP, из которых 96 перекрывались (восемь клеток). Таким образом, 30% пятен флуоресценции Gag-GFP коррелировали со структурами почкования, а 28% топографически обнаруженных почков имели ассоциированную флуоресценцию (фиг. 4 D ). Мы пришли к выводу, что наличие флуоресценции Gag-GFP необходимо для надежного отличия подлинных VLP от других топографически обнаруженных выступов. Для сравнения на рис.4 E и F соответственно.
ТЕМ-изображения иммуномеченых криосрезов показали, что в клетках HeLa только Gag-GFP может продуцировать VLP диаметром до 200 нм (фиг. 4 G ). Это наблюдение согласуется с нашими измерениями SICM и с Müller et al. (6), утверждая, что нет необходимости коэкспрессировать Gag и Gag-GFP для формирования VLP в этих ячейках. Также в соответствии с ранее опубликованными наблюдениями (23) мы иногда наблюдали бутоны Gag, украшающие кончики микроворсинок (рис.4 G , красная стрелка). Это может объяснить ассоциацию флуоресценции Gag-GFP с выступами в виде пальцев на корреляционных изображениях SICM-FCM.
В качестве альтернативы GFP мы также проанализировали Gag с тегами SNAP. SNAP меньше, чем GFP (19,4 кДа против 26,9 кДа), и в этой конструкции вставлен между доменами MA и CA Gag, а не на С-конце. Согласно опубликованным данным, это ослабляет некоторые из стерических ограничений, которые влияют на сборку Gag-GFP, и производит частицы, подобные тем, которые производятся только Gag (6).В клетках HeLa, трансфицированных Gag-SNAP, мы наблюдали отрастание VLP как с неограниченной верхней поверхности клеток, так и с поверхностей, близко противоположных соседним клеткам. VLP и зачатки, сформированные на неограниченной поверхности, выглядели как сферические / изогнутые структуры, подобные описанным выше (рис. 4 H , Top ), хотя некоторые частицы также содержали разрывы в слое Gag (рис. 4 H , рис. Врезка , белая стрелка). Для сравнения, почкующиеся структуры на мембранах той же клетки, близко противоположной соседней, выглядят плоскими (рис.4 H , снизу ). Это может быть связано с различием в биофизических свойствах PM в межклеточных контактах и / или отсутствием внешнего пространства, в котором VLP могут отрастать. Независимо от основной причины, это указывает на то, что кинетика сборки и отпочкования VLPs на базальной поверхности, как измерено с помощью TIRFM, может зависеть от непосредственной близости стеклянной подложки.
Мы попытались проследить образование VLP в живых клетках HeLa, трансфицированных Gag-GFP.Однако нам было трудно надежно идентифицировать и отслеживать отдельные VLP из-за наличия плотных и динамичных микроворсинок и спинных складок.
Формирование VLP в клетках Cos-7.
В отличие от клеток HeLa, в клетках Cos-7 образуется очень мало микроворсинок и дорсальных складок (24, 25), что делает эти клетки более надежными для идентификации других наноструктур, таких как VLP, в топографических исследованиях (12). SICM-изображения клеток Cos-7, зафиксированных через 26 часов после трансфекции h3B-mPlum / Gag ( SI Приложение , рис.S3 A ) выявили многочисленные выступы мембраны, которые напоминали полностью сформированные почки или VLP со средней высотой 100 нм (IQR = от 110 до 90, n = 31) и шириной 100 нм (IQR = от 110 до 90, n ). = 31). И высота, и ширина зачатков, сформированных в клетках Cos-7, были значительно ниже ( P <0,05), чем у VLP, образованных немеченым Gag в клетках Jurkat. Плотность выступов указывает на то, что, подобно клеткам Jurkat, многие VLP остаются прикрепленными к клеточной мембране после завершения сборки.ПЭМ-изображения клеток Cos-7, трансфицированных SynGP, также подтвердили образование похожих на вид VLP в этом типе клеток ( SI Приложение , рис. S3 B , Top ). Подобно клеткам HeLa, зачатки Gag, сформированные в областях межклеточного контакта клеток Cos-7, были плоскими или слегка изогнутыми ( SI Приложение , Fig. S3 B , Bottom ). Покадровые изображения SICM, записанные в клетках Cos-7 через 26 часов после трансфекции с помощью h3B-mPlum / Gag, показали, что, подобно клеткам Jurkat, VLP могут собираться и достигать полного размера за ∼30 с ( SI Приложение , рис.S3 C , красные стрелки). Хотя клетки Cos-7 экспрессируют только низкие уровни тезерина (26), большинство VLP остаются на поверхности клетки в течение десятков минут, постепенно уходя за пределы области наблюдения, что препятствует измерению времени высвобождения. Невозможно было отобразить индуцированное протеазой высвобождение полностью сформированных VLP или образование VLP в присутствии протеазы, поскольку обработка протеазой вызвала быстрые изменения в морфологии клеток с последующей потерей адгезии и округления клеток.
SICM-FCM изображения клеток, фиксированных через 24 часа после трансфекции с помощью Gag-GFP: SynGP 1: 1, выявили как Gag-GFP-положительные зачатки, так и выступы без детектируемой флуоресценции Gag-GFP ( SI Приложение , рис. S3 D , красные и белые стрелки соответственно). Мы идентифицировали в общей сложности 363 пятна флуоресценции Gag-GFP и 123 топографически обнаруженных зачатка VLP, из которых 90 перекрывались (10 клеток), то есть 25% пятен флуоресценции Gag-GFP коррелировали с почковыми структурами и более 70% обнаруживаемых топографически. бутоны имели ассоциированную флуоресценцию ( SI Приложение , рис.S3 E ). Средняя высота Gag-GFP-отрицательных выступов составляла 160 нм (IQR = 200-80, n = 19), что значительно выше ( P <0,001), чем Gag-GFP-положительных зачатков (90 нм, IQR). = От 110 до 45, n = 31), предполагая, что первые могли быть микроворсинками ( SI Приложение , рис. S4 C ). Средние диаметры (115 нм, IQR = от 150 до 90, n = 31) Gag-GFP-положительных выступов были значительно больше диаметров зачатков, образованных немеченым Gag ( P <0.008), предполагая, что в клетках Cos-7 мечение GFP мешает Gag-управляемому образованию VLP. Подтверждая это, ПЭМ-изображения иммуномеченых криосрезов клеток Cos-7 с 1: 1 Gag-GFP: SynGP показали образование плоских и слегка изогнутых сборок Gag ( SI Приложение , рис. S3 F , Top ) или VLP аберрантной формы с разрывами в слое Gag ( SI Приложение , рис. S3 F , Bottom , стрелка). Чтобы определить, представляют ли плоские структуры Gag, наблюдаемые на изображениях фиксированных клеток SICM-FCM и ТЕМ, раннюю стадию почкования, и для измерения времени сборки и высвобождения, мы выполнили покадровую визуализацию SICM-FCM в живых трансфицированных клетках Cos-7. с 1: 1 Gag-GFP: SynGP.В соответствии с наблюдениями в фиксированных клетках, живые изображения SICM-FCM выявили корреляцию между пятнами флуоресценции Gag-GFP и предполагаемыми плоскими или слегка изогнутыми сборками Gag ( SI Приложение , рис. S3 G ) и полностью развитыми зачатками VLP ( SI Приложение , рис. S3 A ). Пятна флуоресценции Gag-GFP, которые коррелировали с плоскими или слегка изогнутыми сборками Gag, имели различное время жизни в диапазоне от 20 с ( SI Приложение , рис. S3 G , белая стрелка) до более 15 минут ( SI Приложение , Инжир.S3 G , красная стрелка). Важно отметить, что мы не наблюдали прогрессивного роста плоских или слегка изогнутых сборок Gag в полностью сформированные почки ( n = 84). Полноразмерные Gag-GFP-положительные выступы также были статичными ( SI Приложение , рис. S4 A ), выдерживали продолжительность наблюдения и имели средний срок службы 1266 ± 571 с ( n = 7). . Для сравнения профили поперечных сечений слегка изогнутых и полностью развитых VLP представлены в Приложении SI , рис.S4 B . Длительное время жизни полноразмерных зачатков предполагает, что они представляют собой либо зачатки, прерванные на поздней стадии сборки, либо полностью собранные и выпущенные VLP, которые остаются прикрепленными к PM. Трансфекция клеток Cos-7 с соотношением Gag-GFP и SynGP 1: 5, а также 1: 1 Vpr-GFP: SynGP также приводила к образованию в основном плоских и слегка изогнутых сборок Gag ( SI Приложение , рис. .S4 D — G ).
Эти данные показывают, что образование VLP немеченым Gag может занять значительно меньше времени, чем предполагалось ранее, и что флуоресцентная маркировка может влиять на формирование структуры VLP.Кроме того, по сравнению с клетками Jurkat, в клетках Cos-7 большинство зачатков оставалось неглубоким, и полностью сформированные VLPs наблюдались редко.
Формирование VLP в клетках HEK293T.
Клетки HEK293T часто используются для получения рекомбинантных инфекционных лентивирусов, поэтому мы также исследовали образование Gag VLP в этих клетках. Топографические изображения SICM клеток, зафиксированных через 20 часов после трансфекции с помощью h3B-mPlum / Gag, выявили выступы PM, которые по размеру и форме напоминали либо полностью сформированные зачатки, либо VLP, прикрепленные к клеточной поверхности (рис.5 А ). Выступы имели среднюю высоту 104 нм (IQR = от 110 до 100, n = 31) и ширину 103 нм (IQR = 115 до 90, n = 31) ( SI Приложение , рис. S5), аналогичны размерам зачатков, образованных немеченым Gag в клетках Cos-7, и значительно ниже ( P <0,05), чем в клетках Jurkat. Обработка клеток протеазой 100 мкг / мл B. licheniformis Субтилизин А привела к быстрому снижению количества выступов на 64 ± 13% (два независимых эксперимента), что указывает на то, что они представляют собой VLP, которые остаются прикрепленными к поверхности клетки после отпочкования. завершено.Сообщается, что, как и Cos-7, экспрессия тезерина не обнаруживается в клетках HEK293T (27). Покадровые изображения клеток SICM, записанные через 25–27 часов после трансфекции, в присутствии протеазы (одна клетка, один эксперимент), выявили активно образующиеся VLP (фиг. 5 B ). Средняя продолжительность жизни почек составляла 36 ± 43 с (рис. 5 C ), что аналогично времени жизни почек, образованных немеченым Gag в клетках Jurkat.
Рис. 5.VLP ВИЧ на клетках HEK293T. ( A ) SICM-изображение VLP на клетке, трансфицированной h3B-mPlum / Gag, зафиксированной через 20 часов после трансфекции.( B ) Покадровые изображения HS-SICM, показывающие образование и исчезновение VLP (красные стрелки) в клетках, записанные, начиная с 8 часов после трансфекции. Изображения были получены со скоростью пять кадров в минуту. ( C ) Распределение времен жизни VLP. ( D ) Корреляционные изображения SICM-FCM почкующихся структур на фиксированных клетках, трансфицированных 1: 5 Gag-GFP: SynGP. ( E ) Диаграмма Эйлера, показывающая перекрытие распределения пятен флуоресценции Gag-GFP и топографически обнаруженных зачатков.( F ) ТЕМ-изображения трансфицированных клеток HEK293T; На изображениях с большим увеличением видны зародыши, сформированные на неограниченных мембранах (1 и 2), и отсутствие зачатков, образованных на мембранах, расположенных близко к соседним клеткам (3). ( G ) ТЕМ-изображение VLP на клетках, трансфицированных только SynGP. (Масштабные полосы: 2 мкм в F , слева и 200 нм в F [панели с большим увеличением] и G .)
Визуализация SICM-FCM клеток HEK293T, трансфицированных 1: 5 Gag-GFP : SynGP показал, что большинство мембранных выступов с ассоциированной флуоресценцией GFP были слегка изогнутыми или полусферическими по форме (рис.5 D ) со средней высотой 54 нм (IQR = от 77,5 до 27,5, n = 52, 5 ячеек) и диаметром 145 нм (IQR = от 150 до 112,5, n = 52, 5 ячеек) ( SI Приложение , рис. S5). Мы идентифицировали в общей сложности 235 пятен флуоресценции Gag-GFP и 155 топографически обнаруженных зачатков VLP, из которых 133 перекрывались (10 клеток), то есть 56% всех пятен флуоресценции Gag-GFP коррелировали с топографически обнаруживаемыми выступами мембраны и только 14% бутоны были GFP-отрицательными (рис.5 E ). В соответствии с SICM-FCM, ПЭМ-изображения показали многочисленные полусферические и случайные бутоны Gag в форме леденцов на неограниченных мембранах (рис. 5 F , панели 1 и 2 с большим увеличением). Однако полностью сформированные VLP, ассоциированные с PM, встречались редко. Мы не наблюдали почкующихся структур на мембранах, близко противоположных соседним клеткам (Fig. 5 F , панель 3). Подобно клеткам Cos-7, трансфекция клеток HEK293T с помощью SynGP подтвердила, что образуются и высвобождаются VLP с формой и размерами, подобными вирусам дикого типа (рис.5 G ).
Трансфекция клеток HEK293T 1: 1 Vpr-GFP: SynGP привела к образованию зачатков (рис.6 A ) со средней высотой 140 нм (IQR = 160-120, n = 43, шесть ячеек) и диаметром 105 нм (IQR = 120-100, n = 43, шесть ячеек) ( SI Приложение , рис. S5). Мы идентифицировали в общей сложности 140 пятен флуоресценции Gag-GFP и 123 топографически обнаруженных зачатка VLP, из которых 117 перекрывались (девять клеток), то есть 84% всех пятен флуоресценции Vpr-GFP коррелировали с топографически обнаруживаемыми выступами мембраны и 95% зачатков. были Gag-GFP-положительными (рис.6 В ). ПЭМ-изображения показали случайные сборки PM Gag, варьирующиеся от плоских до полностью сформированных VLP (рис. 6 C ). На покадровых изображениях SICM-FCM мы также наблюдали значительную корреляцию между топографически обнаруживаемыми почками и флуоресценцией Vpr-GFP (рис.6 D и E ), хотя не всегда было возможно разрешить отдельные пятна флуоресценции, поскольку почки часто были расположены ближе, чем предел оптической дифракции. Хотя нам удалось обнаружить появление новообразованных бутонов (рис.6 D , красные стрелки), а также исчезновение VLP (рис. 6 E , красные стрелки), было невозможно проследить весь путь, так как большинство почек оставалось на поверхности клетки более 30 мин ( n = 22) и смещались в область сканирования и выходили из нее. Некоторые бутоны наблюдались на ПМ до 2 ч. Длительное время пребывания полноразмерных почек либо указывает на то, что они были задержаны на поздней стадии почкования, либо оставались связанными с поверхностью клетки после завершения почкования.
Рис. 6. ОбразованиеVLP ВИЧ в клетках HEK293T, трансфицированных Vpr-GFP и SynGP. ( A ) Корреляционные изображения SICM-FCM VLP на фиксированных клетках HEK293T, трансфицированных 1: 1 Vpr-GFP: SynGP. ( B ) Диаграмма Эйлера, показывающая относительное перекрытие пятен флуоресценции Vpr-GFP с топографически обнаруженными почками. ( C ) ПЭМ-изображения клетки, трансфицированной 1: 1 Vpr-GFP: SynGP, демонстрирующие плоские сборки Gag и высвобожденные VLP (красные стрелки). (Масштаб: 200 нм.) ( D и E ) Покадровые изображения SICM-FCM, показывающие формирование ( D , красные стрелки) и исчезновение VLP ( E , красные стрелки).Изображения получены со скоростью 2 кадра в минуту.
Данные, полученные на клетках HEK293T, предполагают, что флуоресцентное мечение может влиять на структуру VLP и кинетику сборки, что перекликается с результатами, полученными на клетках Cos-7 и Jurkat.
Напряжение клеточной мембраны и вязкость при образовании VLP.
Клеточные мембраны лучше всего описать как двумерный вязкоупругий материал / неньютоновскую жидкость, который при деформации проявляет как вязкие, так и упругие свойства (28, 29). В попытке понять, как биофизические свойства PM влияют на формирование VLP, мы составили карту жесткости клеток с помощью SICM и измерили микровязкость мембран с помощью микроскопии визуализации времени жизни флуоресценции (FLIM) во всех четырех типах клеток, использованных в исследовании.
Ранее было продемонстрировано, что пипетка SICM может использоваться для измерения жесткости клеток и поверхностного натяжения капель без прямого контакта с поверхностью образца. Это может быть достигнуто путем деформации ПМ либо путем использования гидростатического давления для выпуска струи жидкости из наконечника пипетки (30, 31), либо путем использования внутренних сил отталкивания, которые возникают при взаимодействии на близком расстоянии между отрицательно заряженным стеклом пипетки. пипетка и отрицательно заряженная липидная мембрана.Эти взаимодействия происходят при высоких значениях уставки (например, от 2 до 3%) по сравнению с уставкой, обычно используемой для визуализации, то есть от 0,4 до 0,5% падения ионного тока (32, 33). В наших экспериментах мы использовали второй метод, поскольку он позволил нам использовать пипетки меньшего диаметра и тем самым достичь более высокого пространственного разрешения при картировании жесткости клеток. Было показано, что при заданном значении 2% пипетка с апертурой 110 нм оказывает достаточное усилие, чтобы подтолкнуть PM 100 к 200 нм, но недостаточное для деформации нижележащего цитоскелета.Уставка 3% необходима для создания более высокой силы, необходимой для измерения жесткости основной актиновой коры (32). Таким образом, отображение жесткости при малых усилиях может использоваться для отчета о напряжении PM. Мы картировали жесткость контрольных клеток и клеток, трансфицированных h3B-mPlum / Gag, как положительных, так и отрицательных по флуоресценции h3B-mPlum. Типичные изображения топографии клеток и соответствующие карты жесткости клеток, положительных по флуоресценции h3B-mPlum, показаны в Приложении SI, рис. S6 A — D .Статистический анализ показал, что жесткость контрольных клеток Jurkat была значительно ниже, чем жесткость других трех типов клеток, а жесткость клеток HEK293T была ниже жесткости клеток Cos-7 и HeLa (двухвыборочный тест t , P <0,01). Из всех клеточных линий экспрессия Gag значительно снижала жесткость только в клетках HeLa (двухвыборочный тест t , P <0,04) ( SI Приложение , рис. S6 E ).Таким образом, вероятность обнаружения образования флуоресцентно меченных VLP коррелировала с более низким напряжением PM.
Затем мы визуализировали вязкость ТЧ с помощью FLIM, используя молекулярные роторы на основе BODIPY со вставкой мембраны, как описано ранее (34, 35). Было продемонстрировано, что роторы BODIPY локализуются в областях ацильной цепи жидкофазных бислоев (36) и при возбуждении могут либо подвергаться радиационному распаду через испускание флуоресценции, либо распадаться через безызлучательные пути, обычно с участием механизма внутримолекулярного вращения.На скорость этого безызлучательного распада влияет трение, создаваемое окружающей средой, то есть локальная микровязкость (37, 38). Мы получили изображения FLIM, взяв отдельно верхнюю, неприкосновенную мембрану и среднюю (экваториальную) мембрану, где клетки образуют контакты. Невозможно надежно измерить время жизни BODIPY на нижних мембранах вблизи поверхности покровного стекла из-за лазерного рассеяния на границе раздела стекло / жидкость. Репрезентативные FLIM-изображения верхней и средней мембран клеток Jurkat и HEK293T, трансфицированных h3B-mPlum / Gag, показаны в приложении SI , рис.S7 A и C , Левый и Правый соответственно. Мы обнаружили, что вязкость верхних, не соприкасающихся мембран была одинаковой для всех типов клеток ( SI Приложение , рис. S7 F , слева ). Интересно, что, подобно снижению жесткости клеток, экспрессия Gag влияла только на вязкость верхней мембраны в клетках HeLa. Вязкость мембран на межклеточных контактах также была одинаковой для всех типов клеток ( SI Приложение , рис.S7 F , Right ), и экспрессия Gag на него не влияла. Однако, за исключением клеток HeLa, вязкость PM на контактах между клетками была значительно выше, чем вязкость верхних, не соприкасающихся мембран (тест с двумя образцами t , P <0,01). Пример более высокой вязкости мембраны при контакте клетка-клетка в клетках Jurkat показан в приложении SI , рис. S7 A , слева , стрелка. Это хорошо коррелирует с нашим наблюдением, что только плоские или слегка изогнутые структуры Gag наблюдались с помощью ПЭМ на межклеточных контактах.
Обсуждение
Для многих вирусов в оболочке сборка частиц происходит в PM, так что по завершении свободные вирионы высвобождаются во внеклеточное пространство. Несмотря на то, что она признана важным этапом репликации и передачи вируса, динамика образования частиц для большинства вирусов плохо изучена. Для ВИЧ-1 сборка и почкование были подробно изучены с использованием методов флуоресцентной визуализации живых клеток (1–3, 5), которые, по большей части, основаны на визуализации TIRF, когда наблюдаемые частицы формируются на клеточной мембране. рядом со стеклянной подложкой.Хотя этот подход позволяет лучше визуализировать сборку, за счет уменьшения фоновой флуоресценции, контакт со стеклянными поверхностями, как сообщается, влияет на свойства PM, вызывая кластеризацию рецепторов, изменения подвижности (39) и перестройки цитоскелета (40), которые могут влиять на динамику сборка и выпуск вирусов. Таким образом, альтернативные методы, которые могут отображать образование вируса на неприлипающих клеточных поверхностях, могут предоставить дополнительную информацию о сборке и высвобождении вируса. Здесь мы показываем, что SICM-FCM, коррелирующий с HS, можно использовать для визуализации образования немеченых и флуоресцентно меченных VLP на верхней, неприлипающей поверхности трансфицированных клеток.Важно отметить, что этот метод может контролировать не только рекрутирование флуоресцентно меченых вирусных белков в сайты почкования, но также измерять топологические изменения, связанные с деформацией мембраны и высвобождением частиц.
Мы обнаружили, что на не прикрепленной мембране клеток Jurkat, Cos-7 и HEK293T топологические изменения, связанные с образованием VLP, могут происходить всего за 20 секунд. Большинство полностью собранных VLP в клетках Jurkat и HEK293T высвобождаются через 0,5–3 мин после первого обнаружения этих топологических изменений.Хотя недавно было продемонстрировано, что истощение PIP 2 приводит к разборке решеток Gag с клеточной мембраны (16), мы предположили, что сборка Gag в зачатки в физиологических условиях необратима и резкое исчезновение топографически обнаруженных зачатков вместе с ассоциированными флуоресценция представляет собой вылет VLP. Это значительно быстрее, чем сообщалось ранее (1, 3, 5). Хотя ранее сообщалось о пунктах флуоресценции Gag-GFP со временем жизни 33 с, на основании совместной локализации с эндоцитарными маркерами они не считались отпочковывающимися VLP (3).Вопреки нашим ожиданиям, мы не наблюдали постепенного увеличения высоты зачатка в течение ~ 8 минут, что свидетельствовало бы о прогрессивной сборке Gag в VLP с последующим высвобождением частиц через ~ 25 минут после начала сборки в соответствии с ранее опубликованными наблюдениями. (1⇓ – 3, 5, 41, 42). Чтобы сравнить наши измерения с опубликованными данными, мы рассчитали время отпочкования VLP для полных событий с момента первого появления флуоресцентного пятна до момента исчезновения топографически обнаруженных VLP.Среднее время бутонизации составило 248 ± 155 с ( n = 11) в клетках Jurkat, трансфицированных Gag-GFP: SynGP 1: 1, и 113 ± 81 с ( n = 12) в клетках, трансфицированных Vpr-GFP: SynGP. 1: 1, что значительно быстрее, чем публиковалось ранее. Для событий, в которых высвобождение VLP не было зарегистрировано из-за того, что VLP дрейфовали из зоны наблюдения, мы рассчитали временную задержку между первым появлением сигнала флуоресценции и первым появлением топологически обнаруживаемой выпуклости.В 12 из 19 событий, идентифицированных для обеих конструкций, сигналы флуоресценции появлялись одновременно с зачатками. Средняя временная задержка составила 45 ± 99 с ( n = 8) в клетках Jurkat, трансфицированных Gag-GFP: SynGP 1: 1, и 33 ± 60 с ( n = 11) в клетках, трансфицированных Vpr-GFP: SynGP. 1: 1. Для немеченых VLP мы оценили временную задержку следующим образом. Средняя VLP с радиусом r = 60 нм и, следовательно, площадью поверхности, равной 45 239 нм 2 , обычно состоит из 2000-5000 молекул Gag, то есть от 9 до 22.6 нм 2 на молекулу Gag. Площадь поверхности минимальной почки (сферический колпачок, высота = 10 нм) составляет 3,777 нм 2 и содержит от 167 до 419 молекул Gag. Принимая во внимание скорость сборки от 5 до 10 затворов в секунду (43), потребуется от 17 до 84 секунд, чтобы сформировать почку высотой 10 нм, которую можно было бы с уверенностью разрешить с помощью SICM. Это время очень близко к временной задержке между появлением сигнала флуоресценции и первым появлением выпуклости, которую мы измерили экспериментально для меченых VLP.Когда эти временные задержки добавляются к среднему времени бутонизации флуоресцентно меченых и немеченых VLP, рассчитанному на основе топографических данных SICM, время бутонизации все еще значительно меньше, чем ранее опубликовано. Возможно, что в наших экспериментах мы упустили из виду значительную часть частиц с более длительным временем жизни, когда они покидали зону наблюдения. Было обнаружено, что увеличение области сканирования нецелесообразно, так как это приводит к снижению скорости сканирования (недостаток, который характерен для всех методов сканирующей зондовой микроскопии), что препятствует надежному отслеживанию VLP.
Намного более быструю кинетику сборки, которую мы наблюдали, возможно, можно объяснить тем фактом, что мы наблюдали образование VLP на верхних поверхностях ячеек, где сборка не ограничивается непосредственной близостью стеклянной подложки. Хотя сообщалось, что среднее время от начала сборки до высвобождения ВИЧ-1 с дорсальной поверхности клеток, зарегистрированное конфокальной микроскопией с вращающимся диском, было неотличимо от результатов, полученных с помощью TIRFM (1), наши данные ПЭМ показывают плоские заплатки с кляпом в ограниченном пространстве поддерживают идею о том, что свободное пространство может влиять на кинетику сборки вируса.Другая возможность заключается в том, что более длительное время сборки и высвобождения, наблюдаемое при флуоресцентной визуализации, было связано с неспецифическим связыванием вновь образованных VLP с клеточными мембранами (1, 5). Это подтверждается нашим наблюдением, что при обработке протеазой VLP-продуцирующих клеток Jurkat и HEK293T, которые не экспрессируют tetherin или TIM-1, по крайней мере три четверти VLP могут оставаться связанными с поверхностью после завершения сборки.
Мы также обнаружили, что на образование VLP могут влиять методы флуоресцентного мечения, а эффективность образования флуоресцентно меченых частиц может варьироваться в разных типах клеток.Трудно оценить, в какой степени GFP влияет на кинетику образования и высвобождения VLP, поскольку точное соотношение молекул Gag-GFP в каждой почке варьируется. Подход котрансфекции, используемый для предотвращения морфологических дефектов, наблюдаемых в VLP при использовании только Gag-GFP, недавно был тщательно исследован Gunzenhäuser et al. (7). Авторы утверждали, что для данного коэффициента котрансфекции (при использовании более чем одной конструкции) отдельные клетки экспрессируют широкий диапазон соотношений белков и что необходима количественная оценка экспрессии немеченого Gag.Более того, четкой корреляции между количеством немеченого Gag в одной клетке и количеством меченых белков Gag на кластер не сообщалось. В соответствии с этим наши результаты показывают, что хотя кластеры Gag-GFP в клеточных мембранах производят дифракционно-ограниченные флуоресцентные пятна с широтой жизни, это не гарантирует последующее образование топографически обнаруживаемых зачатков и VLP. Хотя снижение pGag_eGFP при котрансфекции с pSynGP вызывало более низкую экспрессию соответствующего белка, судя по флуоресценции GFP, оно не спасало отпочкование VLP в клетках Cos-7 и HEK293T.
Наблюдение за различными свойствами образования VLP в разных типах клеток привело нас к исследованию биофизических свойств PM. Наши данные о жесткости клеток и микровязкости мембран показывают, что сборка топографически обнаруживаемых флуоресцентно меченных VLP более эффективна в более мягких клетках (клетках с более низким натяжением мембраны), таких как Jurkat, и в областях с более низкой вязкостью мембраны и свободным внешним пространством, то есть вдали от них. от межклеточных контактов. Согласно теоретическим моделям, взаимодействие Gag-Gag приводит к линейному натяжению на краю частично сформированного зачатка, которого достаточно, чтобы противодействовать силе, вызванной жесткостью изгиба и натяжением липидной мембраны, что позволяет сборке ВИЧ продолжить свое завершение (44). .Однако жесткость изгиба и вязкость зависят от липидного состава мембраны, на который влияют, например, длина ацильной цепи, содержание холестерина и т. Д., Которые варьируются в разных типах клеток (45, 46). Ранее было продемонстрировано, что время роста почек экспоненциально увеличивается с увеличением вязкости мембраны (44). Следовательно, события сборки могут быть захвачены как частичные зачатки за счет уменьшения притяжения Gag-Gag или за счет увеличения натяжения мембраны. Подобно предыдущим наблюдениям (18), наши данные ПЭМ выявили связанные с GFP разрывы в слое Gag почек и VLP во всех типах клеток, использованных в этом исследовании.Такие неоднородности могут уменьшить силы, генерируемые взаимодействием Gag-Gag, необходимые для противодействия натяжению мембраны и препятствовать сборке VLP. В соответствии с этим, мы обнаружили, что по сравнению с коэкспрессией Gag-GFP и SynGP, где GFP может препятствовать взаимодействию Gag-Gag, трансфекция с помощью Vpr-GFP и SynGP последовательно приводила к более высокой корреляции между топографически обнаруженными почками и флуоресценцией в Jurkat и HEK293T. клетки.
Таким образом, мы показываем, что HS-корреляция SICM-FCM обеспечивает методологию живого изображения формирования вирусных частиц, отпочковывающихся от клеточных PM.Этот подход может быть применен к нормально неприлипающим клеткам, таким как Т-клетки Jurkat, физиологически релевантной модели репликации ВИЧ, а также к множеству адгезивных типов клеток. Используя этот подход, мы обнаружили, что сборка и высвобождение VLP ВИЧ может занимать значительно меньше времени, чем предполагалось ранее, и может варьироваться для разных доменов PM. Наблюдаемая нами кинетика сборки и высвобождения VLP не отличается от кинетики покрытых клатрином везикул, которые, судя по общему количеству вовлеченных молекул, несколько сложнее, чем образование ВИЧ (47, 48).
вирусоподобных частиц (VLP) — Creative Biolabs
Вирусоподобные частицы (VLP)
Creative Biolabs — всемирно известный поставщик услуг для технологии вирусоподобных частиц (VLP). Примечательно, что несколько вакцин-кандидатов на основе VLP были успешно получены с помощью нашей передовой платформы техники VLP. Наши опытные ученые рады предложить лучший сервис и самую качественную продукцию для удовлетворения любых конкретных требований наших клиентов по всему миру.
Вирусоподобные частицы (VLP) — это искусственные белковые структуры, имеющие общую структуру, аналогичную их соответствующим нативным вирусам. Они напоминают вирусы со свойством самосборки, но теряют первоначальную инфекционную способность из-за модификаций генома. VLP симметрично построены из сотен белков оболочки, которые могут быть генетически сконструированы так, чтобы представлять собой регулярное расположение эпитопных цепей в желаемых положениях внешней поверхности. По сравнению с мономерными или олигомерными белками-носителями, VLP способны обеспечивать не только более высокую плотность чужеродных белков на частицу, но также поддерживать характерную трехмерную конформацию, что особенно важно для представления конформационных эпитопов.В настоящее время VLP признаны одними из наиболее многообещающих и широко изученных молекулярных носителей или наночастиц для различных приложений.
С 1980-х годов было сконструировано и охарактеризовано более 100 VLP, происходящих из вирусов микробов, насекомых, растений и млекопитающих. Creative Biolabs предоставляет высококачественные продукты VLP, полученные из различных семейств вирусов, включая VLP HBV, VLP ВИЧ, VLP HPV, VLP CA16, VLP EV71, VLP полиовируса, VLP MERS-CoV, VLP SARS-CoV, VLP SARS-CoV-2, полиомавирусы. VLP, AAV VLP, бактериофаг Qβ VLP, Zika VLP и т. Д.
Одним из важнейших шагов для успешного получения VLP является правильный выбор подходящей системы хозяина экспрессии. В общем, выбор идеальной системы зависит от многих факторов, например: конкретная цель, желаемое количество, последующие приложения и т. д. Creative Biolabs создала широкий спектр хорошо зарекомендовавших себя платформ экспрессии, которые могут соответствовать различным исследовательским и промышленным целям:
- Производство VLP в E. coli Система: E.coli — это наиболее часто используемая система для производства VLP с низкой стоимостью, высоким выходом и быстрым временем обработки.
- Производство VLP в системе дрожжевых клеток: система дрожжевых клеток также является отличной альтернативой в отличие от бактериальной системы, поскольку она способна к посттрансляционным модификациям, таким как гликозилирование или фосфорилирование, и не вызывает проблем с эндотоксинами (особенно для разработки вакцин).
- Производство VLP в системе клеток насекомых: система клеток насекомых — еще одна широко используемая система из-за ее быстрого роста, эффективных посттрансляционных модификаций и легкого масштабирования.
- Производство VLP в растительной системе: система растительных клеток может снизить риск занесения патогенов человека и может производить крупномасштабное производство с низкими затратами.
- Производство VLP в системе клеток млекопитающих: система клеток млекопитающих может как увеличить гибкость и стабильность продукции, так и максимально восстановить нативные эукариотические PTM. Кроме того, эта система может предложить правильное сворачивание и сборку мембранных белков, что продемонстрировало превосходную надежность и высокую вероятность успеха.
Фактически, некоторые вакцины, полученные на основе VLP, используются в коммерческих целях в качестве медицинских продуктов, а другие продукты на основе VLP уже находятся на разных стадиях клинических исследований. Несколько замечательных преимуществ были достигнуты при разработке VLP в качестве инструментов генной терапии и новых наноматериалов для доставки. Вообще говоря, VLP имеют большой потенциал для ряда приложений, включая:
Разработка вакцины: наша команда имеет обширный опыт в разработке и разработке продуктов VLP для доставки интегральных антигенов с обеими ветвями адаптивного иммунитета.Наша вакцинная композиция на основе VLP способна значительно повысить иммуногенность антигена за счет использования адъювантных солей алюминия. Кроме того, будут использоваться специальные методы для уменьшения агрегации консервантов и VLP.
Развитие антител: VLP могут служить совершенным иммуногеном, который может вызывать высокоэффективные иммунные ответы in vivo . Мы успешно получили много связывающих антител с помощью стратегии иммунизации VLP, особенно против вирусных антигенов или мембранных антигенов.
Технология липочастиц: в настоящее время наша команда предоставляет высокоочищенные и стабильные VLP, содержащие большое количество мембранных белков в форме липочастиц, для удовлетворения различных требований, таких как анализы связывания лигандов, скрининг антител и производство иммуногенов.
Системы доставки: наша команда может применять VLP в качестве систем доставки для транспортировки различных соединений, включая ДНК, миРНК, пептиды, белки и лекарства.
Биоимиджинг: наша команда профессионально предоставляет услуги химической модификации VLP, такие как конъюгация зонда для приложений биоимиджинга, как in vivo, и in vitro, , благодаря высокой биологической совместимости VLP.
Нацеливание на клетки: мы можем разработать сложные VLP для обеспечения высокоспецифичного нацеливания на клетки. Доступны альтернативные подходы, включая витамины, пептиды, нуклеиновые кислоты (аптамеры) и углеводные белки (в основном антитела).
Creative Biolabs теперь предлагает ультрасовременную службу вирусоподобных частиц (VLP) на основе нашей уникальной технологической платформы. Наша команда по исследованиям и разработкам состоит из группы инициативных и опытных ученых, которые постоянно стремятся предоставить наиболее профессиональную и удовлетворительную помощь нашим клиентам по всему миру.Не стесняйтесь обращаться к нам для дальнейших обсуждений.
Список литературы
- Ширбагаи, З., и Болхассани, А. (2016). Различные применения вирусоподобных частиц в биологии и медицине: вакцинация и системы доставки. Биополимеры , 105 (3), 113-132.
- Качмарчик С. Дж., Ситараман К., Янг Г. А. и др. (2011). Доставка белка с использованием искусственно созданных вирусоподобных частиц. Proceedings of the National Academy of Sciences , 108 (41), 16998-17003.
- Йозефсберг Дж. О., Бакленд Б. (2012). Технология производства вакцин. Биотехнология и биоинженерия , 109 (6), 1443-1460.
- Луа Л. Х. Л., Коннорс Н. К., Сэйнсбери Ф. и др. (2014). Биоинженерия вирусоподобных частиц в качестве вакцин. Биотехнология и биоинженерия , 111 (3), 425-440.
- Чен Кью, Лай Х. Вирусоподобные частицы растительного происхождения в качестве вакцин (2013). Вирусоподобные частицы растительного происхождения в качестве вакцин. Вакцины и иммунотерапевтические средства для человека , 9 (1), 26-49.
- Яо Л., Ван С., Су С. и др. (2012). Конструирование мультигенной экспрессионной системы бакуловирус-шелкопряд и ее применение для получения вирусоподобных частиц. PloS one , 7 (3), e32510.
- Зелтинс, А. (2013). Конструирование и характеристика вирусоподобных частиц: обзор. Молекулярная биотехнология , 53 (1), 92-107.
- Кушнир Н., Стритфилд С. Дж., Юсибов В.(2012). Вирусоподобные частицы как высокоэффективная платформа для вакцины: разнообразие мишеней и производственных систем, а также достижения в клинической разработке. Вакцина , 31 (1), 58-83.
Все перечисленные услуги и продукты предназначены только для исследовательского использования. Не использовать в диагностических или терапевтических целях.
Белковые клетки и вирусоподобные частицы: от фундаментальных знаний до биомиметической терапии
* Соответствующие авторы
a Кафедра наноинжиниринга, Калифорнийский университет, Сан-Диего, Калифорния , США
б Департамент биоинженерии, Калифорнийский университет, Сан-Диего, Калифорния , США
c Отделение радиологии Калифорнийского университета, Сан-Диего, Калифорния , США
д Онкологический центр Мура, Калифорнийский университет, Сан-Диего, Калифорния , США
и Центр наноиммуноинжиниринга, Калифорнийский университет, Сан-Диего, Калифорния , США
f Школа химической и биомедицинской инженерии, Технологический университет Наньян, Сингапур 637457, Сингапур
г NTU-Северо-западный институт наномедицины, Технологический университет Наньян, Сингапур 637457, Сингапур
ч Центр клеточных фабрик и биополимеров, Институт открытия лекарств Гриффита, Университет Гриффита, Натан, QLD 4111, Австралия
Электронная почта: f.

 Профилактика всегда лучше, чем лечение. Для получения дополнительных сведений посетите сайт www.cancer.orgExternal.
Профилактика всегда лучше, чем лечение. Для получения дополнительных сведений посетите сайт www.cancer.orgExternal.
 Это может занять несколько минут. После завершения нажмите кнопку просмотреть подробные результаты сканирования. Вы должны увидеть троянских: Win32/FakeSysdef перечисленные в области результатов.
Это может занять несколько минут. После завершения нажмите кнопку просмотреть подробные результаты сканирования. Вы должны увидеть троянских: Win32/FakeSysdef перечисленные в области результатов.
Ваш комментарий будет первым